题目内容
18.下列说法或表示法正确的是( )| A. | 等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)→C(金刚石)△H=+1.19 kJ•mol-1可知,石墨比金刚石稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量 | |
| D. | 在101KPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
分析 A、从物质的聚集状态不同,反应热不同来分析,当气体转化为固体时要放出热量;
B、从物质能量高低与稳定性的关系来分析,能量越低物质越稳定;
C、根据中和热的概念以及固体溶于水的过程是放热的过程来判断;
D、据燃烧热的概念:指1mol物质完全燃烧生成稳定化合物时放出的热量来回答.
解答 解:A、白磷蒸气和白磷固体的聚集状态不同,当气体转化为固体时要放出热量,故等量的白磷蒸气和白磷固体分别完全燃烧,白磷放出的热量多,故A错误;
B、由C(S,石墨)═C(S,金刚石);△H=+1.9kJ•mol-1可知,石墨的总能量比金刚石的总能量小低,能量越低物质越稳定,故石墨比金刚石稳定,故B正确;
C、中和热是强酸的稀溶液和强碱的稀溶液中和生成1mol水放出的热量,但是20.0gNaOH固体溶于水的过程还要放出热量,故C错误;
D、燃烧热是指1mol甲烷完全燃烧生成稳定化合物时放出的热量,H是指生成液态水,故D错误.
故选B.
点评 本题考查化学反应与能量问题,为小综合,做题时注意反应热、中和热等问题,本题易错点为硫酸和碱的反应,注意浓硫酸与稀硫酸的区别.

练习册系列答案
相关题目
8.属于铝热反应的是( )
| A. | Al+HCl | B. | Al+H2SO4 | C. | Al+MgO | D. | Al+MnO2 |
6.下列化合物的1H-NMR谱图中吸收峰数目正确的是( )
| A. | CH3CH2CH2CH3(3组) | B. | CH2═CH-CH2CH3(2组) | ||
| C. | 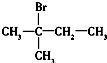 (4组) (4组) | D. | 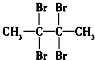 (1组) (1组) |
13.对于下列各组反应,反应开始时,产生氢气速率最快的是( )
| A. | 70℃,将0.1mol 镁粉加入到10mL 6mol•L-1 的硝酸溶液中 | |
| B. | 60℃,将0.2mol 镁粉加入到20mL 3mol•L-1 的盐酸溶液中 | |
| C. | 60℃,将0.1mol 镁粉加入到10mL 3mol•L-1 的硫酸溶液中 | |
| D. | 60℃,将0.2mol 铁粉加入到10mL 3mol•L-1 的盐酸溶液中 |
3.以下关于化学实验中“先与后”的说法中正确的是( )
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体后,先移出导管后撤酒精灯
③制取气体时,先检验装置气密性后装药品
④点燃可燃性气体(如H2、CO等)时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2.
①加热试管时,先均匀加热,后局部加热
②用排水法收集气体后,先移出导管后撤酒精灯
③制取气体时,先检验装置气密性后装药品
④点燃可燃性气体(如H2、CO等)时,先检验气体纯度后点燃
⑤做H2还原CuO实验时,先通H2后加热CuO,反应完毕后,先撤酒精灯待试管冷却后停止通H2.
| A. | ①②③⑤ | B. | ①②④⑤ | C. | ①②③④ | D. | 全部 |
10.下列反应的离子方程式书写正确的是( )
| A. | NaAlO2溶液中通入过量的CO2:2 AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| B. | 磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-═Na2SiO3↓+H2O | |
| C. | 向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2═I2+2H2O | |
| D. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ |
 .
.