题目内容
14. 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A,C,D都是有机物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A,C,D都是有机物.(1)乙醇中官能团的名称是羟基,A的结构简式是CH3CHO;
(2)③的化学方程式是CH3COOH+C2H5OH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O,反应类型是酯化反应或取代反应,浓硫酸的作用是催化剂、吸水剂;
(3)④的反应现象是钠沉在液面下,反应较平稳,有气体生成,放出热量;
(4)对比①和②能得出的结论是醇的燃烧为彻底氧化,而醇的催化氧化是羟基被氧化.
分析 A、C、D都是有机物,由图可知,乙醇发生催化氧化生成A为CH3CHO,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成C为CH3COOCH2CH3,乙醇与钠发生反应生成D为CH3CH2ONa,反应②是乙醇燃烧生成二氧化碳和水,据此解答.
解答 解:A、C、D都是有机物,由图可知,乙醇发生催化氧化生成A为CH3CHO,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成C为CH3COOCH2CH3,乙醇与钠发生反应生成D为CH3CH2ONa,反应②是乙醇燃烧生成二氧化碳和水.
(1)乙醇中含有的官能团为羟基,A的结构简式为:CH3CHO,
故答案为:羟基;CH3CHO;
(2)反应③是CH3CH2OH和CH3COOH在浓硫酸作用下反应生成CH3COOCH2CH3,反应方程式为:为CH3COOH+C2H5OH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O,属于酯化反应或取代反应,浓硫酸其催化剂、吸水剂作用,
故答案为:为CH3COOH+C2H5OH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O;酯化反应或取代反应;催化剂、吸水剂;
(3)反应④是乙醇与钠发生反应生成CH3CH2ONa与氢气,反应现象是:钠沉在液面下,反应较平稳,有气体生成,放出热量,
故答案为:钠沉在液面下,反应较平稳,有气体生成,放出热量;
(4)对比①和②能得出的结论是:醇的燃烧为彻底氧化,而醇的催化氧化是羟基被氧化,
故答案为:醇的燃烧为彻底氧化,而醇的催化氧化是羟基被氧化.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸、酯的性质与转化,难度不大,有利于基础知识的巩固.

练习册系列答案
相关题目
4.下列物质按酸,碱,盐,有机物,混合物顺序排列的是( )
| A. | 硝酸,苛性钠,明矾,淀粉,氯水 | |
| B. | 碳酸钠,盐酸,食盐,酒精,合金 | |
| C. | 醋酸,纯碱,碳酸钙,硝基苯,石油 | |
| D. | 氢溴酸,消石灰,高锰酸钾,硝基苯,石油 |
5. 对碳硫及其化合物的研究有重要的意义.
对碳硫及其化合物的研究有重要的意义.
I.利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ.mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ.mol-1
③CO(g)+H2O(g)═CO2+H2(g)△H=-41.3kJ.mol-1
写出利用水煤气合成二甲醚(CH3OCH3) 的热化学方程式:3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
Ⅱ.工业制硫酸的过程中利用反应2SO2(g)+O2(g)$?_{加热}^{催化剂}$SO3(g)△H=-196.6kJ•mol-1,将SO2转化为SO3,尾气SO3可用NaOH溶液进行吸收.请回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=$\frac{c{\;}^{2}(SO{\;}_{3})}{c{\;}^{2}(SO{\;}_{2})•c(O{\;}_{2})}$.
(2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,下列说法中正确的是BC(填字母).
A.若反应速率v正(O2)=2v逆(SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,再充入2mol SO2和1mol O2,n(SO3)/n(SO2)增大
C.平衡后移动活塞压缩气体,达到平衡时SO2、O2的百分含量减小,SO3的百分含量增大
D.平衡后升高温度,平衡常数K增大
(3)将一定量的SO2(g)和O2(g)分别通入到容积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验1从开始到反应达到化学平衡时,v(SO2)表示的反应速率为0.2mol/L•min;T1>T2(选填“>”“<”或“=”),理由是反应放热,温度升高平衡向左移动,反应物转化率低
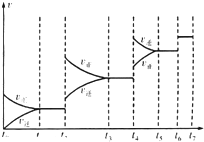
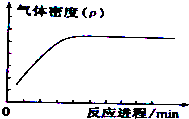
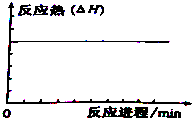
(4)某SO2(g)和O2(g)反应体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图所示.若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是升高温度;图中表示平衡混合物中SO2的转化率最高的一段时间是t3~t4.
 对碳硫及其化合物的研究有重要的意义.
对碳硫及其化合物的研究有重要的意义.I.利用水煤气合成二甲醚(CH3OCH3)的三步反应如下:
①2H2(g)+CO(g)═CH3OH(g)△H=-90.8kJ.mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ.mol-1
③CO(g)+H2O(g)═CO2+H2(g)△H=-41.3kJ.mol-1
写出利用水煤气合成二甲醚(CH3OCH3) 的热化学方程式:3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
Ⅱ.工业制硫酸的过程中利用反应2SO2(g)+O2(g)$?_{加热}^{催化剂}$SO3(g)△H=-196.6kJ•mol-1,将SO2转化为SO3,尾气SO3可用NaOH溶液进行吸收.请回答下列问题:
(1)写出该反应的化学平衡常数表达式:K=$\frac{c{\;}^{2}(SO{\;}_{3})}{c{\;}^{2}(SO{\;}_{2})•c(O{\;}_{2})}$.
(2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,下列说法中正确的是BC(填字母).
A.若反应速率v正(O2)=2v逆(SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,再充入2mol SO2和1mol O2,n(SO3)/n(SO2)增大
C.平衡后移动活塞压缩气体,达到平衡时SO2、O2的百分含量减小,SO3的百分含量增大
D.平衡后升高温度,平衡常数K增大
(3)将一定量的SO2(g)和O2(g)分别通入到容积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | X | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | Y | t |
(4)某SO2(g)和O2(g)反应体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图所示.若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是升高温度;图中表示平衡混合物中SO2的转化率最高的一段时间是t3~t4.
6.硫铁矿是工业制硫酸的主要原料,某硫铁矿中含FeS2,假设杂质不参与反应,用酸性高锰酸钾溶液滴定法测定硫铁矿的纯度,其反应原理:FeS2+3MnO4-+8H+═3Mn2++Fe3++2SO42-+4H2O.取x g该样品磨成粉末滴加c mol•L-1酸性高锰酸钾溶液至恰好完全反应,消耗酸性高锰酸钾溶液V mL.则该样品的纯度为( )
| A. | $\frac{cV}{x}$×100% | B. | $\frac{cV}{25x}$×100% | C. | $\frac{40cV}{x}$×100% | D. | $\frac{cV}{4x}$×100% |
3.中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.关于${\;}_{116}^{293}$Lv的叙述错误的是( )
| A. | 原子序数116 | B. | 中子数177 | C. | 核外电子数116 | D. | 相对原子质量293 |
3.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A | B | C | D |
| 除去Cl2中的HCl | 制取少量纯净的CO2气体 | 分离CCl4萃取碘水后已分层的有机层和水层 | 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
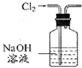 | 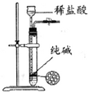 | 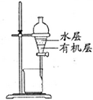 | 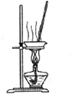 |
| A. | A | B. | B | C. | C | D. | D |


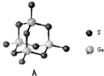 某化合物由阳离子[(CH3)4 N]+和阴离子A按个数比4:1组成,阴离子A的结构如图所示:
某化合物由阳离子[(CH3)4 N]+和阴离子A按个数比4:1组成,阴离子A的结构如图所示: