题目内容
19.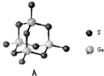 某化合物由阳离子[(CH3)4 N]+和阴离子A按个数比4:1组成,阴离子A的结构如图所示:
某化合物由阳离子[(CH3)4 N]+和阴离子A按个数比4:1组成,阴离子A的结构如图所示:(1)S原子以sp3杂化轨道与Ge结合.
(2)阴离子A的化学式为[Ge4S10]4-.
分析 (1)由图可知S原子形成2个共价键,结合S原子的最外层电子数判断其价层电子对数;
(2)阴离子A中含有4个Ge和10个S,其中4个S只形成一个共价键,则还要得到一个电子才能形成8电子稳定结构.
解答 解:(1)S原子的最外层电子数为6,由图可知S原子形成2个共价键,则阴离子A中S原子含有2个成键电子对和2个孤电子对,即其价层电子对数为4,属于sp3杂化;
故答案为:sp3;
(2)阴离子A中含有4个Ge和10个S,其中4个S只形成一个共价键,则还要得到一个电子才能形成8电子稳定结构,则A离子带有4个负电荷,即离子的化学式为[Ge4S10]4-,故答案为:[Ge4S10]4-.
点评 本题考查了杂化理论的应用、微粒化学式的确定,题目难度不大,注意把握价层电子对数的判断方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列关于甲烷,乙烯,乙醇,乙酸的说法中,不正确的是( )
| A. | 乙烯可以使溴水褪色,发生加成反应 | |
| B. | 甲烷和氯气在光照条件下反应,反应类型为取代反应 | |
| C. | 乙醇在铜作催化剂并加热条件下生成乙醛,发生还原反应 | |
| D. | 生活中可以用食醋出去水壶中的水垢,主要是利用食醋中醋酸的酸性 |
4.生活中处处有化学,下列说法不正确的是( )
| A. | 采用原煤脱硫技术,可减少燃煤时产生的SO2 | |
| B. | 食品中适量添加防腐剂,可以保障安全 | |
| C. | 垃圾分为可回收物、厨余垃圾、有害垃圾、其它垃圾等,废旧电池属于可回收垃圾 | |
| D. | 用红薯酿酒的过程中包含氧化还原反应 |
8.将Na、Na2O、NaOH、Na2S、Na2SO4分别加热熔化,需要克服相同类型作用力的物质有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
8.SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀.针对上述一系列变化,下列说法错误的是( )
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述反应可知氧化性HNO3>Fe3+>稀硫酸 | |
| C. | 上述过程中,会产生一种无色、难溶于水的气体 | |
| D. | 若通入的SO2完全反应,则通入的SO2和逸出的气体物质的量之比为1:1 |
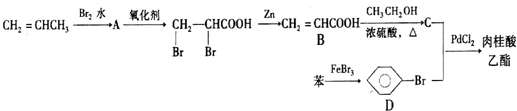
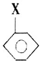 +CH2═CHCOOCH3$\stackrel{PdCl_{2}}{→}$
+CH2═CHCOOCH3$\stackrel{PdCl_{2}}{→}$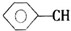 =CHCOOCH3+HX(X为卤素原子)
=CHCOOCH3+HX(X为卤素原子)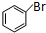 +CH2=CHCOOCH2CH3$\stackrel{PdCl_{2}}{→}$
+CH2=CHCOOCH2CH3$\stackrel{PdCl_{2}}{→}$ +HBr.
+HBr.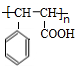 .
. 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A,C,D都是有机物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A,C,D都是有机物.