题目内容
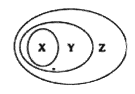
【题目】NaC1O2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下: 
回答下列问题:
(1)“电解”所用食盐水由粗盐水精制而成,精制对,为除去Mg2+和Ca2+ , 要加入的试剂分别为、 .
(2)写出“反应”步骤中生成ClO2的化学方程式 .
(3)实验所用原料硫酸是由浓硫酸稀释而获得,写出实验过程 .
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2 . 此吸收反应中,氧化剂与还原剂的物质的量之比为 .
(5)将lmolSO2和lmolC12通入水中形成lL的溶液,所得溶液中氢离子浓度为mol/L.
【答案】
(1)NaOH溶液;Na2CO3溶液
(2)2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2
(3)将浓硫酸沿着烧杯壁慢慢的注入水里,并不断搅拌
(4)2:1
(5)4
【解析】解:(1)食盐溶液中混有Mg2+ 和Ca2+ , 可以利用过量NaOH溶液除去Mg2+ , 利用过量Na2CO3溶液除去Ca2+ , 所以答案是:NaOH溶液;Na2CO3溶液;(2)“反应”步骤中生成ClO2的化学方程式为2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2 , 所以答案是:2NaClO3+SO2+H2SO4=2NaHSO4+2ClO2;(3)实验所用原料硫酸是由浓硫酸稀释而获得,写出实验过程为将浓硫酸沿着烧杯壁慢慢的注入水里,并不断搅拌,所以答案是:将浓硫酸沿着烧杯壁慢慢的注入水里,并不断搅拌;(4)由图可知,利用含过氧化氢的氢氧化钠溶液吸收ClO2 , 产物为ClO2﹣ , 则此反应中ClO2为氧化剂,还原产物为ClO2﹣ , 化合价从+4价降为+3价,H2O2为还原剂,氧化产物为O2 , 每摩尔H2O2得到2mol电子,依据电子守恒可知氧化剂和还原剂的物质的量之比为2:1,所以答案是:2:1;(5)lmolSO2和lmolC12通入水中形成lL的溶液,发生Cl2+SO2+2H2O=H2SO4+2HCl,则生成硫酸为1mol,生成HCl为2mol,所得溶液中氢离子浓度为 ![]() =4mol/L,所以答案是:4.
=4mol/L,所以答案是:4.

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案【题目】乙二酸俗名草酸,易溶于水,其水溶液与酸性KMnO4溶液反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)本实验滴定达到终点的标志是__________________________;
(3)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(4)若滴定终点时俯视滴定管刻度,则x值会______(填“偏大”、“偏小”或“不变”)。
【题目】根据表中提供的数据(25 ℃),判断下列说法正确的是
化学式 | 电离常数 |
HClO | Ka=3.0×10-8 |
H2CO3 | Ka1=4.3×10-7 |
Ka2=5.6×10-11 |
A. 向氯水中加入硫酸,可增强杀菌效果
B. 温度升高,次氯酸的电离常数增大
C. 25 ℃时,ClO-的水解常数为3.0×10-6
D. 要提高氯水中HClO的浓度,可加入足量的Na2CO3固体