��Ŀ����
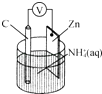
����Ŀ��������֮���ת����ϵ��ͼ������������ʡ�ԣ�C��D����X��Y��Z������Ԫ����ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�ǿ�ȼ�����壬GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ�ٳ���������ӡˢ��·�壮��ش��������⣺
��1��GԪ�������ڱ��е�λ�� �� C�ĵ���ʽ ��
��2���Ƚ�Y��Z��ԭ�Ӱ뾶��С������дԪ�ط��ţ���
��3��д��E����ȩ��Ӧ�Ļ�ѧ��Ӧ����ʽ���л����ýṹ��ʽ��ʾ������Ӧ���ͣ� ��
��4��д��ʵ�����Ʊ�G�����ӷ�Ӧ����ʽ ��
��5������D��NaOH��Һ��Ӧ������������P��Q����P��Na����������Ϊ43%��������Ϊ ��
��6��ʵ�����м���L��Һ�е������ӳ�ѡ����Һ�������� ��
��7��A�а���X��Y��ZԪ�أ�A�Ļ�ѧʽΪ
��8���о�����������D��һ�������¿ɱ���ԭΪ��Ө���ľ���N����ṹ��ԭ�ӵ�����Ϊ�������壬��д��N����1��ͬ��������������� ��
���𰸡�
��1���������ڵڢ���A�壻![]()
��2��C��O
��3��CH3CHO+2Cu��OH��2 ![]() CH3COOH+Cu2O��+2H2O��������Ӧ
CH3COOH+Cu2O��+2H2O��������Ӧ
��4��MnO2+4H++2Cl�� ![]() ?Mn2++Cl2��+2H2O
?Mn2++Cl2��+2H2O
��5���մ�
��6��KSCN��Һ����Һ����Ѫ��ɫ
��7��Cu2��OH��2CO3��Cu��OH��2?CuCO3
��8�����ʯ����ʯī����ϩ��C60��
���������⣺X�����ڱ��е�ԭ�Ӱ뾶��С��ΪHԪ�أ�Y��Zԭ������������֮��Ϊ10����X��Y��Z��ԭ�������������������Ƴ�D����H��C��O�е�����Ԫ����ɣ���ɫ�ǿ�ȼ�����壩ΪCO2 �� ����֪��X��Y��Z��H��C��O����CΪH2O��HΪHCl��I��Ư�����ã�ӦΪHClO��dz��ɫ���ػ�ɫ��ҺΪFe2+��Fe3+ �� ��֪JΪFe��KΪFeCl2 �� LΪFeCl3 �� GΪ����ɫ�������壬ӦΪCl2 �� ��Ӧ����������ӡˢ��·��ΪFeCl3��Cu����MΪCu��BΪCuCl2 �� E���������Ƿ�Ӧ��ӦΪCu��OH��2 �� FΪCu2O����A+H��HCl��=B��CuCl2��+C��H2O��+D��CO2����֪��A�Ǻ���Cu2+��̼���Σ���A+H��HCl��=B��CuCl2��+C��H2O��+D��CO2����֪��A�Ǻ���Cu2+��̼���Σ�ӦΪCuCO3��Cu2��OH��2CO3��Cu��OH��2CuCO3 �� A�а���X��Y��ZԪ�أ�A�Ļ�ѧʽΪCu2��OH��2CO3��Cu��OH��2CuCO3 �� ��1��GΪCl2 �� GԪ�������ڱ��е�λ���ǵ������ڵڢ���A�壬CΪH2O��C�ĵ���ʽΪ ![]() �����Դ��ǣ��������ڵڢ���A�壻
�����Դ��ǣ��������ڵڢ���A�壻 ![]() ����2��Y��Z�ֱ���C��O������ͭ����ԭ�Ӱ뾶���μ�С�жϣ�C��O��ԭ�Ӱ뾶C��O�����Դ��ǣ�C O����3��EΪCu��OH��2 �� E����ȩ��Ӧ�Ļ�ѧ��Ӧ����ʽΪ CH3CHO+2Cu��OH��2
����2��Y��Z�ֱ���C��O������ͭ����ԭ�Ӱ뾶���μ�С�жϣ�C��O��ԭ�Ӱ뾶C��O�����Դ��ǣ�C O����3��EΪCu��OH��2 �� E����ȩ��Ӧ�Ļ�ѧ��Ӧ����ʽΪ CH3CHO+2Cu��OH��2 ![]() CH3COOH+Cu2O��+2H2O����Ӧ����Ϊ������Ӧ�����Դ��ǣ�CH3CHO+2Cu��OH��2
CH3COOH+Cu2O��+2H2O����Ӧ����Ϊ������Ӧ�����Դ��ǣ�CH3CHO+2Cu��OH��2 ![]() CH3COOH+Cu2O��+2H2O��������Ӧ�� ��4��ʵ������Ũ������������̷�Ӧ�Ʊ���������Ӧ�����ӷ�Ӧ����ʽΪMnO2+4H++2Cl��
CH3COOH+Cu2O��+2H2O��������Ӧ�� ��4��ʵ������Ũ������������̷�Ӧ�Ʊ���������Ӧ�����ӷ�Ӧ����ʽΪMnO2+4H++2Cl�� ![]() Mn2++Cl2��+2H2O�����Դ��ǣ�MnO2+4H++2Cl��
Mn2++Cl2��+2H2O�����Դ��ǣ�MnO2+4H++2Cl�� ![]() Mn2++Cl2��+2H2O�� ��5��DΪCO2 �� CO2��NaOH��Һ��Ӧ������������ΪNaHCO3��Na2CO3 �� ��Na2CO3��Na����������Ϊ43%��������Ϊ�մ����Դ��ǣ��մ� ��6��LΪFeCl3 �� ʵ�����м���L��Һ�е������ӳ�ѡ��KSCN��Һ����������Һ����Ѫ��ɫ�����Դ��ǣ�KSCN��Һ����Һ����Ѫ��ɫ�� ��7����������ķ�����֪��A�Ļ�ѧʽΪCu2��OH��2CO3��Cu��OH��2CuCO3 �� ���Դ��ǣ�Cu2��OH��2CO3��Cu��OH��2CuCO3�� ��8��CO2���Ի�ԭ����������ṹ�ľ���N�������ϼ۽��ͣ���Ȼ�����˽��ʯ������ͬ�����������Ϊ��̼�ĵ��ʣ�ͬ�������������Ϊ��ʯī������ϩ��C60���� ���Դ��ǣ����ʯ��ʯī����ϩ��C60����
Mn2++Cl2��+2H2O�� ��5��DΪCO2 �� CO2��NaOH��Һ��Ӧ������������ΪNaHCO3��Na2CO3 �� ��Na2CO3��Na����������Ϊ43%��������Ϊ�մ����Դ��ǣ��մ� ��6��LΪFeCl3 �� ʵ�����м���L��Һ�е������ӳ�ѡ��KSCN��Һ����������Һ����Ѫ��ɫ�����Դ��ǣ�KSCN��Һ����Һ����Ѫ��ɫ�� ��7����������ķ�����֪��A�Ļ�ѧʽΪCu2��OH��2CO3��Cu��OH��2CuCO3 �� ���Դ��ǣ�Cu2��OH��2CO3��Cu��OH��2CuCO3�� ��8��CO2���Ի�ԭ����������ṹ�ľ���N�������ϼ۽��ͣ���Ȼ�����˽��ʯ������ͬ�����������Ϊ��̼�ĵ��ʣ�ͬ�������������Ϊ��ʯī������ϩ��C60���� ���Դ��ǣ����ʯ��ʯī����ϩ��C60����