题目内容
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,X比Y的原子系数小1,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
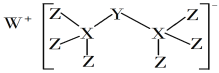
A.Y原子能形成四核18电子的电中性分子
B.元素非金属性的顺序为X>Y>Z
C.W的单质与氧气反应不能产生含共价键的化合物
D.该新化合物中Y不满足最外层8电子稳定结构
【答案】A
【解析】
该化合物由阴、阳离子构成,说明它是离子化合物。从该化合物的结构式看出,W为金属元素;1个Z原子形成1个共价键,说明Z原子最外层有1个或7个电子;1个X原子形成4个共价键,说明X原子最外层有4个电子;Y原子形成2个共价键,阴离子得1个电子,说明Y原子最外层有5个电子;Z核外最外层电子数是X核外电子数的一半,则Z为Cl,X为Si元素;W、X、Y、Z为同一短周期元素,则W为Na,Y为P,据此解答。
根据分析可知,W、X、Y、Z分别为Na、Si、P、Cl元素。
A.Y为P,PH3为四核18电子的电中性分子,故A正确;
B.X、Y、Z分别为Si、P、Cl,同周期从左到右,元素的非金属性逐渐增强,故非金属性X<Y<Z,故B错误;
C.W为Na,Na和氧气在点燃条件下生成Na2O2,含有共价键,故C错误;
D.2个硅原子和1个P原子形成2个共价键,阴离子得到1个电子,所以该化合物中磷原子最外层达到8电子稳定结构,故D错误。
答案选A。

练习册系列答案
相关题目