题目内容
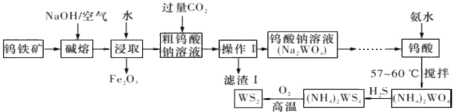
【题目】二硫化钨(WS,WS2中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其主要成分是FeWO4,还含少量Al2()3)制备二硫化钨的工艺流程如图所示,下列说法正确的是
A.操作I中用到的玻璃仪器只有漏斗、烧杯
B.FeWO4在碱熔过程中发生反应的化学方程式为4FeWO4+O2+8NaOH![]() 2Fe2O3+4NaWO3+4H2O
2Fe2O3+4NaWO3+4H2O
C.生成二硫化钨的化学方程式为(NH4)2WS4+3O2![]() 2WS2+4NH3+2S2-+2SO2+2H2O,若生成124g WS2,则该反应所转移的电子数目为2NA
2WS2+4NH3+2S2-+2SO2+2H2O,若生成124g WS2,则该反应所转移的电子数目为2NA
D.滤渣I的主要成分是氢氧化铝,CO2可以用过量盐酸代替
【答案】B
【解析】
由流程可知,钨酸亚铁和氢氧化钠、氧气反应生成氧化铁和钨酸钠,Al2O3和NaOH反应生成NaAlO2,水浸时,可除去不溶于水的氧化铁,向粗钨酸钠溶液中通入过量CO2,经过滤后得到的滤液含钨酸钠,滤渣I的主要成份是Al(OH)3,滤液再经酸化得钨酸,向钨酸中加入氨水并控制温度得钨酸铵,继续通入H2S气体,生成(NH4)2WS4,最后将(NH4)2WS4在氧气中高温加热即可得到WS2;
A. 操作Ⅰ为过滤,需要的玻璃仪器有玻璃棒、漏斗、烧杯,故A错误;
B. FeWO4在碱熔过程中被空气中氧气氧化,生成Fe2O3、Na2WO4和H2O,发生反应的化学方程式为4FeWO4+O2+8NaOH![]() 2Fe2O3+4NaWO3+4H2O,故B正确;
2Fe2O3+4NaWO3+4H2O,故B正确;
C. 生成二硫化钨的化学方程式为(NH4)2WS4+3O2![]() 2WS2+4NH3+2S2-+2SO2+2H2O,(NH4)2WS4中+6价W被还原为+4价的WS2,2价S元素被氧化成0价的S单质,每生成2molWS2转移了4mol电子,同时参加反应的氧气为3mol,则反应中共转移16mol电子,124gWS2的物质的量为:
2WS2+4NH3+2S2-+2SO2+2H2O,(NH4)2WS4中+6价W被还原为+4价的WS2,2价S元素被氧化成0价的S单质,每生成2molWS2转移了4mol电子,同时参加反应的氧气为3mol,则反应中共转移16mol电子,124gWS2的物质的量为:![]() =0.5mol,转移电子的物质的量为:16mol×
=0.5mol,转移电子的物质的量为:16mol×![]() =4mol,即转移电子数目为4NA,故C错误;
=4mol,即转移电子数目为4NA,故C错误;
D. 滤渣I的主要成分是氢氧化铝,氢氧化铝是两性氢氧化物,可以强酸反应,是滤渣溶解,不能用盐酸代替CO2,故D错误;
答案选B。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案