题目内容
16.重铬酸钾是一种应用广泛的氧化剂,某实验小组模拟工业法,用铬铁矿(主要成分为FeO、Cr2O3)为原料制取重铬酸钾(K2Cr2O7),主要流程如图.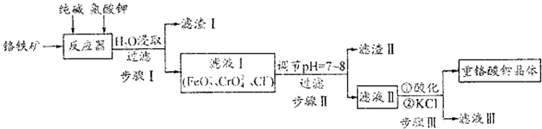
试回答下列问题:
(1)铬铁矿在反应前进行粉碎的目的是增大接触面积,加快反应速率.
(2)通过反应器得到的氧化产物是FeO2-、CrO42-.
(3)步骤Ⅲ酸化时与CrO42-有关的离子方程式力2CrO42-+2H+?Cr2O72-+H2O;该步骤中加入KC1析出大量重铬酸钾晶体,其原理是K2Cr2O7的溶解度小于Na2Cr2O7,发生复分解反应.
(4)滤渣Ⅰ、Ⅱ均要用水多次洗涤,并回收洗涤液,目的是提高原料利用率、防止重金属污染.
(5)酒驾检测时,酸性K2Cr2O7将乙醇最终氧化成乙酸,同时颜色由橙色变为绿色.
分析 铬铁矿主要成分为FeO、Cr2O3,在反应器中与纯碱、氯酸钾反应,由滤液I含有离子可知,Cl元素发生还原反应得到Cl-,而Fe元素、Cr元素均发生氧化反应得到FeO2-、CrO42-,滤液I调节pH后过滤得到滤液Ⅱ,滤液Ⅱ酸化、加入KCl,过滤分离得到重铬酸钾晶体与滤液Ⅲ,则调节PH=7~8目的是使FeO2-转化为Fe(OH)3而除去,步骤Ⅲ酸化目的是将CrO42-转化为Cr2O72-,加入KCl可以使溶解度大的Na2Cr2O7转化为溶解度小的K2Cr2O7.
(1)铬铁矿在反应前进行粉碎,可以增大接触面积,加快反应速率;
(2)根据元素化合价变化判断氧化产物;
(3)由上述分析可知,步骤Ⅲ酸化目的是将CrO42-转化为Cr2O72-,加入KCl使溶解度大的Na2Cr2O7转化为溶解度小的K2Cr2O7;
(4)滤渣附着的物质中含有Cr元素,用水洗涤并回收洗涤液,可以提高原料利用率,防止重金属污染;
(5)酒驾检测时,酸性K2Cr2O7将乙醇最终氧化成乙酸,同时颜色由橙色变为绿色.
解答 解:铬铁矿主要成分为FeO、Cr2O3,在反应器中与纯碱、氯酸钾反应,由滤液I含有离子可知,Cl元素发生还原反应得到Cl-,而Fe元素、Cr元素均发生氧化反应得到FeO2-、CrO42-,滤液I调节pH后过滤得到滤液Ⅱ,滤液Ⅱ酸化、加入KCl,过滤分离得到重铬酸钾晶体与滤液Ⅲ,则调节PH=7~8目的是使FeO2-转化为Fe(OH)3而除去,步骤Ⅲ酸化目的是将CrO42-转化为Cr2O72-,加入KCl可以使溶解度大的Na2Cr2O7转化为溶解度小的K2Cr2O7.
(1)铬铁矿在反应前进行粉碎,可以增大接触面积,加快反应速率,
故答案为:增大接触面积,加快反应速率;
(2)反应中Fe元素化合价由-2价升高为FeO2-中+3价,Cr元素化合价由+3价升高为CrO42-中+6价,故氧化产物为:FeO2-、CrO42-,
故答案为:FeO2-、CrO42-;
(3)由上述分析可知,步骤Ⅲ酸化目的是将CrO42-转化为Cr2O72-,反应离子方程式为:2CrO42-+2H+?Cr2O72-+H2O,K2Cr2O7的溶解度小于Na2Cr2O7,发生复分解反应,加入KC1析出大量重铬酸钾晶体,
故答案为:2CrO42-+2H+?Cr2O72-+H2O;K2Cr2O7的溶解度小于Na2Cr2O7,发生复分解反应;
(4)滤渣附着的物质中含有Cr元素,用水洗涤并回收洗涤液,可以提高原料利用率,防止重金属污染,
故答案为:提高原料利用率,防止重金属污染;
(5)酒驾检测时,酸性K2Cr2O7将乙醇最终氧化成乙酸,同时颜色由橙色变为绿色,
故答案为:乙酸;橙.
点评 本题考查物质制备实验,涉及对操作与原理的分析评价、物质的分离提纯等,关键是根据工艺流程理解制备原理,是对学生综合能力的考查,难度中等.

| A. | 11.5g/mol | B. | 24.3g/mol | C. | 48.4g/mol | D. | 16.2g/mol |
| A. | 未加醋酸时:c(OH-)=c(Na+) | |
| B. | 加入10mL醋酸时:c(OH-)>c(Na+)>c(CH3COO-)>c(H+) | |
| C. | 加入醋酸至溶液pH=7时:c(CH3COO-)=c(Na+) | |
| D. | 加入20mL醋酸时:2c(OH-)=c(CH3COO-)+2c(H+) |
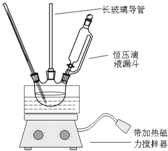 硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:
硝基苯是重要的精细化工原料,是医药和染料的中间体制备,还可做有机溶剂.制备硝基苯的过程如下:①配制混酸:组装如图反应装置.取100mL烧杯,用20mL浓硫酸与浓硝酸18mL配制混和酸,加入漏斗中.把18mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50-60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.
已知(1)
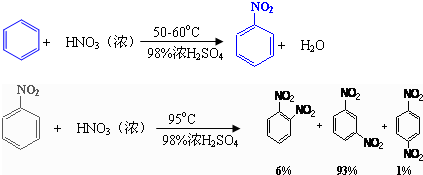
(2)可能用到的有关数据列表如下
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | / | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | / | 338 | 1.84 | 易溶于水 |
(1)配置混酸应先在烧杯中先加入浓硝酸.
(2)恒压滴液漏斗的优点是可以保持漏斗内压强与发生器内压强相等,使漏斗内液体能顺利流下.
(3)实验装置中长玻璃管可用冷凝管(球形冷凝管或直行冷凝管均可)代替(填仪器名称).
(4)反应结束后产品在液体的下层(填“上”或者“下”),分离混酸和产品的操作方法为分液.
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?取最后一次洗涤液,向溶液中加入氯化钙,无沉淀生成,说明已洗净.
(6)为了得到更纯净的硝基苯,还须先向液体中加入氯化钙除去水,然后蒸馏.
 锰锌软磁铁氧体具有高磁导率、低矫顽力和低功率损耗等性能,已广泛应用于电子工业.碳酸锰主要用于制备锰锌软磁铁氧体,而制碳酸锰的原料之一是二氧化锰.某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰.
锰锌软磁铁氧体具有高磁导率、低矫顽力和低功率损耗等性能,已广泛应用于电子工业.碳酸锰主要用于制备锰锌软磁铁氧体,而制碳酸锰的原料之一是二氧化锰.某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰.①将干电池剖切、分选得到黑色混合物(主要成分为MnO2)洗涤、过滤、烘干.
②将上述固体按固液体积比2:9加入浓盐酸、加热,反应完全后过滤、浓缩.
③向上述溶液中加入Na2CO3溶液,边加边搅拌,再过滤即可得到碳酸锰.
(l)在第②步中,将上述固体与浓盐酸混合的目的是将MnO2还原成Mn2+
(2)有人认为,将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成.请写出加入NH4HCO3溶液时发生的离子反应方程式Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(3)查阅文献,发现第③步中,除生成MnCO3外还有可能生成Mn(OH)2,已知Mn(OH)2暴露在空气中时间稍长,易被氧化成褐色的MnO(OH)2,MnCO3和MnO(OH)2受热最终均分解成MnO2,该小组对上述沉淀的成分提出以下假设,请帮助完成假设:
假设一:全部为MnCO3;
假设二:全部为Mn(OH)2;
假设三:既有MnCO3又有Mn(OH)2
为验证假设二是否正确,该小组进行了以下研究:
①定性研究:请你完成表中的内容.
| 实验步骤(不要求写出具体步骤) | 预期的实验现象和结论 |
| 将所得沉淀过滤、洗涤, 将沉淀充分暴露于空气中,观察颜色 | 颜色变成褐色,说明含有Mn(OH)2 |
| 取少量沉淀于试管中,加入足量的盐酸,观察现象 | 没有气泡生成,说明不含MnCO3 |

| A. | 该分子中所有氢原子不可能在同一平面上 | |
| B. | 1mol该物质与氢气反应,最多消耗4mol氢气 | |
| C. | 加入FeCl3溶液呈紫色,因为该物质含有酚类结构特征 | |
| D. | 滴入酸性高锰酸钾溶液,紫色褪去,可证明结构存在碳碳双键 |
| A. | 反应物和生成物的状态 | B. | 是否使用催化剂 | ||
| C. | 一步完成还是多步完成 | D. | 反应的快慢 |
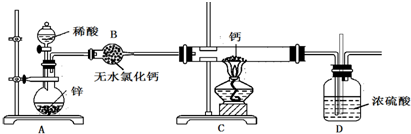

 乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是:
乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是: