题目内容
1. 锰锌软磁铁氧体具有高磁导率、低矫顽力和低功率损耗等性能,已广泛应用于电子工业.碳酸锰主要用于制备锰锌软磁铁氧体,而制碳酸锰的原料之一是二氧化锰.某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰.
锰锌软磁铁氧体具有高磁导率、低矫顽力和低功率损耗等性能,已广泛应用于电子工业.碳酸锰主要用于制备锰锌软磁铁氧体,而制碳酸锰的原料之一是二氧化锰.某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰.①将干电池剖切、分选得到黑色混合物(主要成分为MnO2)洗涤、过滤、烘干.
②将上述固体按固液体积比2:9加入浓盐酸、加热,反应完全后过滤、浓缩.
③向上述溶液中加入Na2CO3溶液,边加边搅拌,再过滤即可得到碳酸锰.
(l)在第②步中,将上述固体与浓盐酸混合的目的是将MnO2还原成Mn2+
(2)有人认为,将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成.请写出加入NH4HCO3溶液时发生的离子反应方程式Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(3)查阅文献,发现第③步中,除生成MnCO3外还有可能生成Mn(OH)2,已知Mn(OH)2暴露在空气中时间稍长,易被氧化成褐色的MnO(OH)2,MnCO3和MnO(OH)2受热最终均分解成MnO2,该小组对上述沉淀的成分提出以下假设,请帮助完成假设:
假设一:全部为MnCO3;
假设二:全部为Mn(OH)2;
假设三:既有MnCO3又有Mn(OH)2
为验证假设二是否正确,该小组进行了以下研究:
①定性研究:请你完成表中的内容.
| 实验步骤(不要求写出具体步骤) | 预期的实验现象和结论 |
| 将所得沉淀过滤、洗涤, 将沉淀充分暴露于空气中,观察颜色 | 颜色变成褐色,说明含有Mn(OH)2 |
| 取少量沉淀于试管中,加入足量的盐酸,观察现象 | 没有气泡生成,说明不含MnCO3 |
分析 (1)在第②步中,将含有MnO2的固体与浓盐酸混合加热发生反应:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O可以使MnO2还原转化为Mn2+;
(2)③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成为二氧化碳气体;
(3)根据题目信息可知:沉淀的成分可能全部为MnCO3,可能全部为Mn(OH)2,还可能是MnCO3和Mn(OH)2;
①根据Mn(OH)2暴露在空气中时间稍长,易被氧化成褐色的MnO(OH)2来分析有无Mn(OH)2;根据MnCO3能与盐酸反应放出气体来分析有无MnCO3;
②固体质量最小值是15.8g是MnO的质量,在300℃以后,通过质量增加量为MnO氧化为MnO2,求出MnO的质量,进而求出含有MnO2的质量;由于Mn(OH)2暴露在空气中时间稍长,易被氧化成褐色的MnO(OH)2,分解得到MnO2,根据MnO2的质量求出Mn(OH)2的质量,从而求出MnCO3质量;
解答 解:(1)在第②步中,将上述固体与浓盐酸混合的目的是利用浓盐酸还原二氧化锰为锰离子;
故答案为:将MnO2还原成Mn2+;
(2)将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成为二氧化碳气体,反应的离子方程式为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
故答案为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
(3)根据题目信息可知:沉淀的成分可能全部为MnCO3,可能全部为Mn(OH)2,还可能是MnCO3和Mn(OH)2,所以有三种假设:假设一:全部为MnCO3;假设二:全部为Mn(OH)2;假设三:既有MnCO3又有Mn(OH)2;
故答案为:既有MnCO3又有Mn(OH)2;
①将所得沉淀过滤、洗涤将沉淀充分暴露于空气中,观察颜色,颜色变成褐色,说明含有Mn(OH)2;另取少量沉淀于试管中,加入足量的盐酸,观察现象,没有气泡生成,说明不含MnCO3.为此证明固体是Mn(OH)2;
故答案为:
| 实验步骤(不要求写出具体步骤) | 预期的实验现象和结论 |
| 将沉淀充分暴露于空气中,观察颜色 | 颜色变成褐色,说明含有Mn(OH)2 |
| 取少量沉淀于试管中,加入足量的盐酸,观察现象 | 没有气泡生成,说明不含MnCO3 |
故答案为:300℃以后,质量增加量为MnO氧化为MnO2 ,计算可得MnCO3质量为11.5(或MnO(OH)2的质量为10.5g),所以既有MnCO3又有Mn(OH)2;
点评 本题主要考查物质的制取、成分的检验、氧化还原反应原理、离子方程式的书写的知识,题目综合性较强,注意题目信息的提取与运用,难度较大.

①NaOH溶液 ②铜丝 ③液态HCl ④盐酸 ⑤Ba(OH)2 ⑥氨气 ⑦氨水 ⑧SO2 ⑨胆矾晶体 ⑩熔融NaCl⑪蔗糖晶体⑫酒精溶液⑬碳酸钙
| 符合的条件 | 序号 | |
| 1 | 混合物 | |
| 2 | 电解质,但熔融状态下并不导电 | |
| 3 | 电解质,但难溶于水 | |
| 4 | 非电解质 | |
| 5 | 既不是电解质,也不是非电解质,但能导电 |
| A. | 1mol O的质量为16g•mol-1 | |
| B. | 1mol He约含有6.02×1023个原子 | |
| C. | 2H既表示2个氢原子,又表示2mol氢原子 | |
| D. | 1mol HCl约含有6.02×1023个原子 |
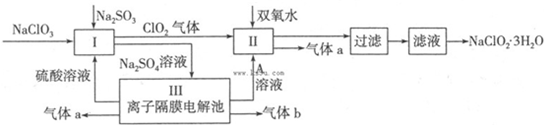
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O;
②常温下,Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-28;Ksp(PbS)=2.4×10-28
(1)反应I中发生反应的离子方程式为SO32-+2ClO3-+2H+=2C1O2+SO42-+H2O.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是bdc(填写序号).
a.蒸馏 b.蒸发浓缩 c.过滤 d.冷却结晶 e.灼烧
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | H2CO3 | H2S |
| Ka/mol•L-1 | 1×10-2 | 6.3×10-4 | K1=4.30×10-7 K2=5.60×10-11 | K1=9.1×10-8 K2=l.1×10-12 |
②Na2S是常用的沉淀剂.某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;常温下,当最后一种离子沉淀完全时(该离子浓度为10-5mol•L-1)此时体系中的S2-的浓度为6.3×10-13mol/L.
(4)Ⅲ装置中生成气体a的电极反应式2H2O-4e-=O2↑+4H+,若生成气体a的体积为1.12L(标准状况),则转移电子的物质的量为0.2mol.
| A. | 150 mL 2 mol•L-1盐酸 | B. | 150 mL 2 mol•L-1硫酸 | ||
| C. | 500 mL 3 mol•L-1盐酸 | D. | 500 mL 18.4 mol•L-1浓硫酸 |
| A. | 标准状况下22.4LNO2中分子数约为NA个 | |
| B. | 常温下,18g${\;}_{\;}^{18}$O2中含有个NA氧原子 | |
| C. | 31g白磷中含的共价键数为3NA | |
| D. | 25℃时pH=13的NaOH溶液中含有0.1NAOH- |
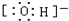 B
B E
E