题目内容
某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下: 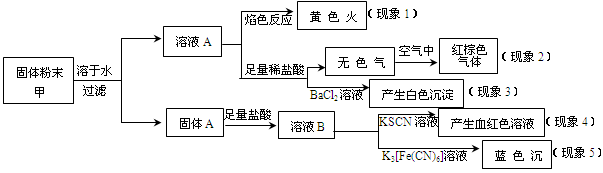
该同学得出的结论正确的是
| A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素 |
| B.根据现象2可推出该固体粉末中一定含有NaNO2 |
| C.根据现象3可推出该固体粉末中一定含有Na2SO4 |
| D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3 |
D
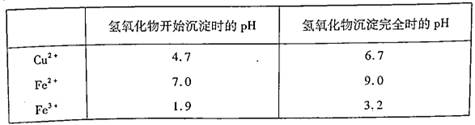
解析试题分析:钠的焰色反应为黄色,故一定含钠元素,观察钾的焰色反应须透过钴玻璃,避免钠的干扰,故无法确定是否含钾,故A错误;红棕色为NO2,则原混合物中可能含有硝酸钠或NaNO2或两者都存在,故B错误;C.K2SO3,在酸性条件下发生氧化还原反应生成SO42-,加入氯化钡生成硫酸钡沉淀,则不一定含硫酸钠,可能有K2SO3,故C错误;溶液B加KSCN溶液呈血红色,说明含有Fe3+,加铁氰化钾显蓝色,证明含亚铁离子,所以该固体含有FeO和Fe2O3.故D正确;故选D。
考点:本题考查物质的检验和鉴别的实验方案的设计,侧重于元素化合物知识的综合运用,题目难度中等。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
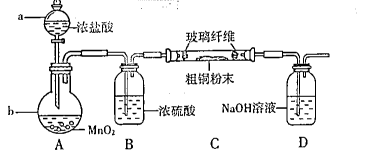
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为________;仪器b中可选择的试剂为________;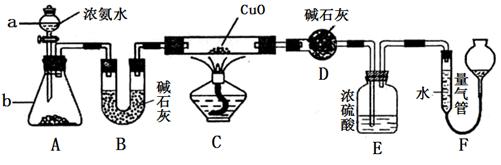
(2)实验室中利用下列各组物质,进行喷泉实验,不能成功的是( )
| A.Cl2与饱和食盐水 | B.CO2 与40%的NaOH溶液 |
| C.NH3与饱和食盐水 | D.HCl与水 |
(4)E装置中浓硫酸的作用_______________________
(5)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为________(用含m、n字母的代数式表示)
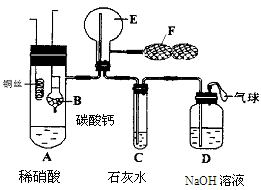
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
|
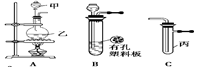
 请按要求填空:
请按要求填空:(1)利用B装置可制取的气体有 (填2种)。
A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入 NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
(2)请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由。
。
(3)请利用上述A、C装置设计一个简单的实验,验证Cl2和Br2的氧化性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
。
B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
(4)B中发生反应的化学方程式为 。
(5)欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是
。
(6)试管丁中的NO2与一定量的O2混合后倒插水中,试管9/10充满水,则原试管丁中的混合气体的平均分子量可能为 。(保留二位小数)
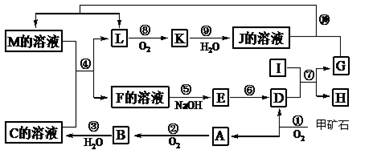
化学美无处不在,下图是物质间发生化学反应的颜色变化,其中X是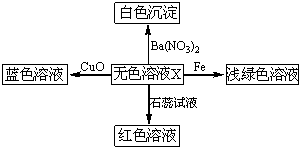
| A.稀盐酸 | B.Na2SO4溶液 | C.稀硫酸 | D.Na2CO3溶液 |
已知X、Y、Z、W均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物已略)。下列说法不正确的是( )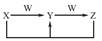
| A.X、Y、Z中至少有一种相同的元素,该元素可以是金属元素也可以是非金属元素 |
| B.物质W可能是化合物,也可能是单质 |
| C.上述转化关系中不可能出现置换反应 |
| D.若X、Y、Z中均含有一种常见金属元素,则W可能是强酸也可能是强碱 |