题目内容
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·xH2O)。
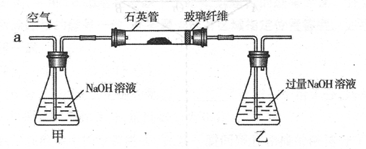
(1)实验室采用如图所示装置,可使粗铜与Cl2反应转化为固体1(部分加热仪器和夹持装置已略去)。该装置中仪器a的名称是 。装置b中发生反应的离子方程式是 。该装置存在一定的安全隐患,消除该安全隐患的措施是 。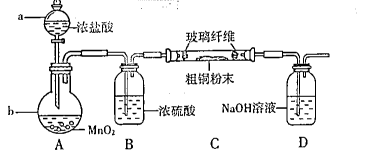
(2)操作Ⅱ中应控制的pH范围为 ,其目的是 。
已知: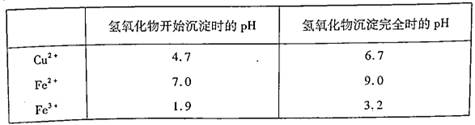
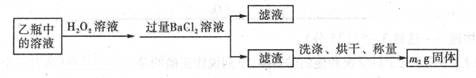
(3)操作Ⅲ的程序依次为 、 、过滤、自然干燥.得到CuCl2·xH2O晶体。
(4)若制备的氯化铜晶体经检验含有FcCl2,其原因可能是 ,试提出两种不同的改进方案:① ;② 。
(15分)(1)分液漏斗(2分);MnO2+4H++2Cl-Mn2++Cl2↑+2H2O(2分);在C和D之间连接一个防倒吸装置(2分);
(2)3.2≤pH<4.7(2分);使FeCl3转化为Fe(OH)3沉淀而与CuCl2溶液分离(或除去CuCl2溶液中FeCl3) (2分) (3)蒸发浓缩、冷却结晶(2分)
(4)与粗铜反应的氯气不足量(1分);①通足量的氯气(1分) ②在操作Ⅱ中加入CuO前先加入足量的H2O2或通入Cl2(1分)
解析试题分析:(1)根据仪器的结构特点可知,仪器A是分液漏斗;装置A是制取氯气的,二氧化锰与浓盐酸发生反应生成氯化锰、氯气、水,则b中反应离子方程式为MnO2+4H++2Cl-Mn2++Cl2↑+2H2O;浓盐酸易挥发,生成的氯气中含有氯化氢,氯气和氯化氢都极易被氢氧化钠溶液吸收,所以需要在C和D之间连接一个防倒吸装置。
(2)根据铁离子和铜离子的沉淀pH值可知,要使铜离子留在溶液中,而使铁离子完全沉淀,需要控制溶液的pH值是3.2≤pH<4.7。
(3)操作Ⅲ的目的是得到氯化铜晶体,所以正确的操作顺序是蒸发浓缩、冷却结晶、过滤、自然干燥.得到CuCl2·xH2O晶体。
(4)若制备的氯化铜晶体经检验含有FcCl2,这说明在反应中氯气是不足的,过量的铁与铁离子反应生成了亚铁离子,所以改进的方法是通足量的氯气或在操作Ⅱ中加入CuO前先加入足量的H2O2或通入Cl2。
考点:考查仪器识别;氯气的制备;实验方案设计与评价;物质的分离与提纯等

 阅读快车系列答案
阅读快车系列答案某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下: 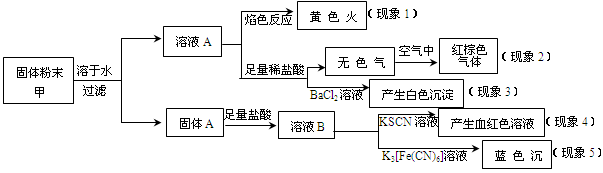
该同学得出的结论正确的是
| A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素 |
| B.根据现象2可推出该固体粉末中一定含有NaNO2 |
| C.根据现象3可推出该固体粉末中一定含有Na2SO4 |
| D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3 |
已知:甲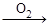 乙
乙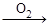 丙
丙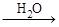 丁,其中丁为强酸,则甲不可能为
丁,其中丁为强酸,则甲不可能为
| A.N2 | B.C | C.S | D.NH3 |
元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化(其中m≠n,且均为正整数)。下列说法正确的是 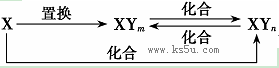
| A.X一定为金属元素 | B.X、Y不可能均为非金属元素 |
| C.若X为Fe,Y可为Cl、Br、但不能是I | D.若X为Fe,Y只能为Cl |
 5CaCl2 + Ca(ClO3)2 + 6H2O
5CaCl2 + Ca(ClO3)2 + 6H2O

 = 。
= 。
 CO2↑+2SO2↑+2H2O,其中浓H2 S04所起的作用是 (填“氧化剂”或“还原剂”)。若有0.2mol碳的完全反应,则消耗H2S04的质量是 g,标况下产生SO2的体积为______________L。
CO2↑+2SO2↑+2H2O,其中浓H2 S04所起的作用是 (填“氧化剂”或“还原剂”)。若有0.2mol碳的完全反应,则消耗H2S04的质量是 g,标况下产生SO2的体积为______________L。
 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2