题目内容
铜和镁的合金4.7克完全溶于浓硝酸中,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已经折算成标准状况)。在反应后的溶液中加入足量的NaOH溶液,生成沉淀的质量为
| A.9.02g | B.8.26g | C.8.61g | D.7.04g |
C
根据题意最终生成的沉淀是氢氧化铜和氢氧化镁,由于金属失去电子的物质的量就是金属阳离子结合的OH-的物质的量。NO2和N2O4分别是0.2mol和0.015mol,所以反应中转移电子是0.2mol+0.015mol×2=0.23mol,则结合的OH-的质量是0.23mol×17g/mol=3.91g,所以沉淀的质量是3.91g+4.7g=8.61g,答案选C。

练习册系列答案
相关题目
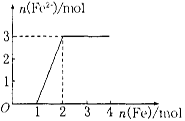
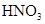 和
和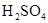 物质的量浓度分别为
物质的量浓度分别为 和
和 ,向该溶液中加入1.92g铜粉,加热,待充分反应后,所得溶液中
,向该溶液中加入1.92g铜粉,加热,待充分反应后,所得溶液中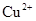 物质的量浓度(
物质的量浓度(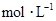 )为( )
)为( ) 5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。
5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。 若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。