��Ŀ����
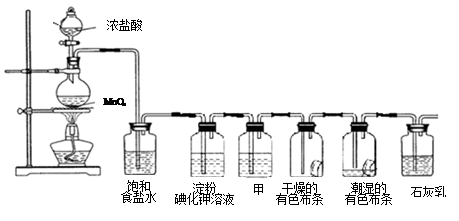
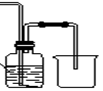
ij��ѧ�С���������ͼ��ʾ(���ּг�װ������ȥ)ʵ��װ�ã���̽����ʪ��Cl2��Na2CO3��Ӧ�õ��Ĺ������ʡ�
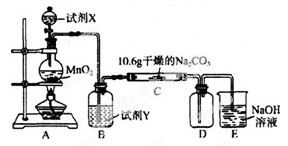
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ�� ��
��2��д���Լ�Y������_____________________��
��3����֪��ͨ��һ�������������D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ�����壬��Ϊ�������������ȷ������C�к��е�����ֻ��һ�֣��Һ���NaHCO3���ֶ�C�ɷֽ��в����̽����
������������裺
����һ���������ֳɷ֣�NaHCO3��__________
��������������ֳɷ֣�NaHCO3��__________��__________��
����Ʒ���������ʵ�顣��д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ��ɲ���������
��ѡʵ���Լ�������������ˮ��ϡ���ᡢBaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���
��4����֪C����0.1 mol Cl2�μӷ�Ӧ��������һ����������֪C�з�Ӧ�Ļ�ѧ����ʽΪ ��
��5��������Na2CO3��NaHCO3��Ϊ0.1mol/L�Ļ����Һ�У�c(OH��)-c(H+)=____ ���ú�̼Ԫ�ص�����Ũ�ȱ�ʾ�����ڸ���Һ�еμ�ϡ����������ʱ����Һ�����ʵijɷ���___________��

��1��д��װ��A�з�����Ӧ�����ӷ���ʽ�� ��
��2��д���Լ�Y������_____________________��
��3����֪��ͨ��һ�������������D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ�����壬��Ϊ�������������ȷ������C�к��е�����ֻ��һ�֣��Һ���NaHCO3���ֶ�C�ɷֽ��в����̽����
������������裺
����һ���������ֳɷ֣�NaHCO3��__________
��������������ֳɷ֣�NaHCO3��__________��__________��
����Ʒ���������ʵ�顣��д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ��ɲ���������
��ѡʵ���Լ�������������ˮ��ϡ���ᡢBaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡC�е�����������Ʒ���Թ��У��μ���������ˮ�������ܽ⣬Ȼ��������Һ�ֱ�����A��B�Թ��С� | |
| ����2����A�Թ��еμ�_________�� | ��������������֤�������в���̼���ƣ� ������Һ����ǣ�֤�������к���̼���ơ� |
| ����3����B�Թ��еμ�________�� | ����Һ����ǣ���ϲ���2�еĢ٣������һ��������ϲ���2�еĢڣ������������� |
��4����֪C����0.1 mol Cl2�μӷ�Ӧ��������һ����������֪C�з�Ӧ�Ļ�ѧ����ʽΪ ��
��5��������Na2CO3��NaHCO3��Ϊ0.1mol/L�Ļ����Һ�У�c(OH��)-c(H+)=____ ���ú�̼Ԫ�ص�����Ũ�ȱ�ʾ�����ڸ���Һ�еμ�ϡ����������ʱ����Һ�����ʵijɷ���___________��
��1��MnO2+4H++2Cl-=Mn2++Cl2��+2H2O
��2������ʳ��ˮ
��3��NaCl��NaCl��Na2CO3��BaCl2��Һ��AgNO3��Һ��
��4��2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O
��5��[c��HCO3-��+3c��H2CO3��+��CO32-��]/2
��2������ʳ��ˮ
��3��NaCl��NaCl��Na2CO3��BaCl2��Һ��AgNO3��Һ��
��4��2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O
��5��[c��HCO3-��+3c��H2CO3��+��CO32-��]/2
��1������̽������������̼���Ʒ�Ӧ��Aװ��Ϊ�������Ʊ�װ�ã����������ӷ���ʽΪ��MnO2+4H+ +2Cl- =Mn2+ +Cl2��+2H2O��
��2��Ũ�����ӷ������������л���HCl���壬Bװ��Ϊ����װ�ã��Լ�ѡ�ñ���ʳ��ˮ��Һ��
��3��������Ӧ���õIJ�����ֻ��һ�����Σ�������NaHCO3���������NaCl���ʣ�����һΪNaHCO3��NaCl������������ֳɷֱַ���NaHCO3
�����ʵ�������֤��Ӧ���跨֤��NaCl��Na2CO3�Ĵ��ڣ���ͨ������Cl-��CO32-�Ĵ��ڡ����������������IJ��裬����2��CO32-�ļ��飬��˿�ѡ��BaCl2��Һ�����������ɫ������˵����Na2CO3�Ĵ��ڣ����������������˵��û��Na2CO3�Ĵ��ڣ�����3Ϊ���������ӵĴ��ڣ����ѡ����������Һ������а�ɫ��������˵��NaCl�Ĵ��ڣ�����û�У��ٽ�ϲ���2���ۼ��������
��2��Ũ�����ӷ������������л���HCl���壬Bװ��Ϊ����װ�ã��Լ�ѡ�ñ���ʳ��ˮ��Һ��
��3��������Ӧ���õIJ�����ֻ��һ�����Σ�������NaHCO3���������NaCl���ʣ�����һΪNaHCO3��NaCl������������ֳɷֱַ���NaHCO3
�����ʵ�������֤��Ӧ���跨֤��NaCl��Na2CO3�Ĵ��ڣ���ͨ������Cl-��CO32-�Ĵ��ڡ����������������IJ��裬����2��CO32-�ļ��飬��˿�ѡ��BaCl2��Һ�����������ɫ������˵����Na2CO3�Ĵ��ڣ����������������˵��û��Na2CO3�Ĵ��ڣ�����3Ϊ���������ӵĴ��ڣ����ѡ����������Һ������а�ɫ��������˵��NaCl�Ĵ��ڣ�����û�У��ٽ�ϲ���2���ۼ��������

��ϰ��ϵ�д�
�����Ŀ
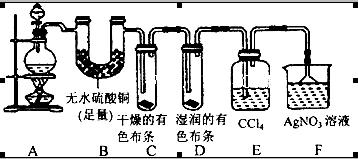
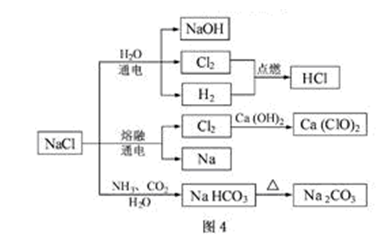


 MnCl2 + C12��+ 2 H2O����
MnCl2 + C12��+ 2 H2O����