题目内容
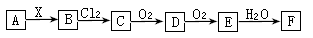
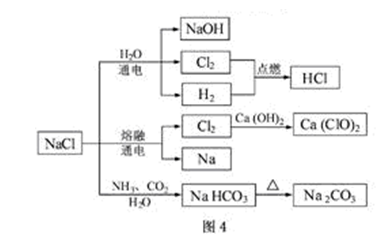
NaCl是一种化工原料,可以制备一系列物质(见图4)。下列说法正确的是

| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.图4所示转化反应都是氧化还原反应 |
B
本题考查元素化合物知识综合内容,拓展延伸至电解饱和食盐水、电解熔融氯化钠、侯氏制碱等内容,但落点很低,仅考查NaHCO3、Na2CO3的溶解度、工业制漂白粉、干燥的Cl2贮存和基本反应类型。重基础、重生产实际应该是我们高三复习也应牢记的内容。25℃,NaHCO3在水中的溶解度比Na2CO3的要小;石灰乳与Cl2的反应中氯发生歧化反应,Cl2既是氧化剂,又是还原剂;常温下干燥的Cl2能用钢瓶贮存仅代表常温Cl2不与铁反应,加热、高温时可以反应;在侯氏制碱法中不涉及氧化还原反应。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目