题目内容
15.在恒温下的密闭容器中,有可逆反应N2+3H2?2NH3(该反应放热),不能说明已达到平衡状态的是( )| A. | 正反应生成的NH3速率和逆反应生成N2的速率相等 | |
| B. | 反应器中压强不随时间变化而变化 | |
| C. | 1molN≡N键断裂的同时,有6molN-H键断裂 | |
| D. | 混合气体平均分子量保持不变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、化学平衡状态时,正反应生成的NH3速率和逆反应生成N2的速率的2倍,故A错误;
B、随着反应的进行体系压强逐渐减小,容器内压强保持不变说明达平衡状态,故B正确;
C、1molN≡N键断裂,等效于6molN-H键形成的同时,有6molN-H键断裂,达平衡状态,故C正确;
D、混合气体平均分子量保持不变,说明物质的量不变反应达平衡状态,故D正确;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
5.有A、B两种有机物各取1mol在足量氧气中充分燃烧,分别生成7mol和3molCO2.只要A、B的总物质的量一定,不论A、B以任意物质的量之比混合,或只要A、B的总质量一定,不论A、B以任意质量之比混合,充分燃烧后生成水的量为一定值,已知A是苯的同系物,则B的分子式为( )
| A. | C3H6O | B. | C3H8O3 | C. | C3H8O2 | D. | C3H8O |
6.某有机物的分子式为C3H6O,通过核磁共振氢谱分析有3个峰,峰面积比例为1:2:3,则该物质可能是( )
| A. | CH3COCH3 | B. | CH3CH2CHO | C. | CH2=CH-CH2OH | D. | CH2=CH-O-CH3 |
10.已知一个N2O3分子的质量为a g,一个N2O5分子的质量为b g,若以一个氧原子质量的$\frac{1}{6}$作为相对原子质量的标准,则NO2的相对分子质量为( )
| A. | $\frac{3(a+b)}{b-a}$ | B. | $\frac{16(b+a)}{b-a}$ | C. | $\frac{8(b-a)}{b+a}$ | D. | $\frac{16(b-a)}{b+a}$ |
7.过氧化钠可作为氧气的来源.常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了14g,反应中有关物质物理量正确的是(NA表示阿伏加德罗常数) ( )
| 二氧化碳 | 碳酸钠 | 转移的电子 | |
| A | 0.5mol | NA | |
| B | 53g | 0.5mol | |
| C | 53g | NA | |
| D | 11.2L | 0.5mol |
| A. | A | B. | B | C. | C | D. | D |
4.下列性质的递变规律不正确的是( )
| A. | F、O、N非金属性依次减弱,HF、H2O、NH3沸点依次降低 | |
| B. | Li、Na、K、Rb、Cs的失电子能力逐渐增强 | |
| C. | Al3+、Mg2+、Na+的离子半径依次增大 | |
| D. | HF、HCl、HBr、HI稳定性依次减弱,还原性依次增强 |
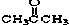 ③CH3CH2Br④
③CH3CH2Br④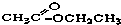 ⑤
⑤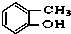 ⑥
⑥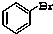
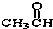 ⑧
⑧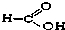 ⑨
⑨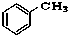 ⑩
⑩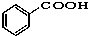
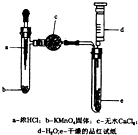 某化学实验小组为探究氯气漂白原理,设计了以下实验装置:
某化学实验小组为探究氯气漂白原理,设计了以下实验装置: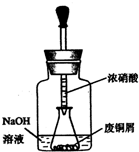 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: