题目内容
6. 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、ClO-、AlO2- |
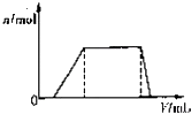
分析 开始加入NaOH没有沉淀和气体产生,则一定有H+,则无ClO-、AlO2-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe2+、Fe3+,有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则有NH4+,据此进行解答.
解答 解:根据图象,开始加入NaOH没有沉淀和气体产生,则一定有H+;后来有沉淀产生且最后消失,则一定没有Mg2+、Fe2+、Fe3+,有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则有NH4+;现象无法知道有无K+,因为有H+,则无ClO-、AlO2-,
综上所述,则该溶液中确定含有的离子是H+、Al3+、NH4+; 一定不含有的阳离子是Mg2+、Fe2+、Fe3+;一定不存在的阴离子是ClO-、AlO2-,
故答案为:H+、Al3+、NH4+; Mg2+、Fe2+、Fe3+;ClO-、AlO2-.
点评 本题考查离子共存及推断,为高频考点,题目难度中等,把握实验中发生的反应及离子的检验方法为解答的关键,侧重分析与逻辑推理能力的考查,注意图象与反应的对应关系及反应的先后顺序.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
1.已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列说法正确的是( )
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列说法正确的是( )
| A. | H2(g)的燃烧热为571.6 kJ•mol-1 | |
| B. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | |
| D. | 3H2(g)+CO2(g)═CH3OH(l)+H2O(l)△H=+131.4 kJ•mol-1 |
11.下列有机物中,既能使溴水褪色,也能使酸性高锰酸钾溶液褪色,还能使蓝色石蕊试纸变红的是( )
| A. | 丙烯酸 | B. | 甲酸乙酯 | C. | 甲苯 | D. | 乙酸 |
15.类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列说法正确的是( )
| A. | Na、Mg与水反应产生碱和氢气,Fe与在一定条件下水反应也生成碱和氢气 | |
| B. | CaC2能水解:CaC2+2H2O═Ca(OH)2+C2H2↑;则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3↓+3CH4↑ | |
| C. | Fe能置换硫酸铜溶液的铜;则Na也能置换硫酸铜溶液的铜 | |
| D. | 工业上电解熔融MgCl2的制取金属镁;则也可以用电解熔融AlCl3的制取金属铝 |
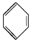 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$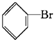 +HBr.
+HBr.
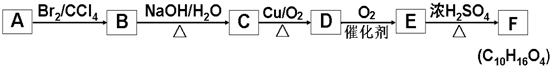
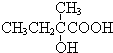
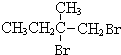 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$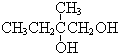 +2NaBr,反应类型取代反应
+2NaBr,反应类型取代反应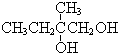 +O2+O2$\stackrel{催化剂}{→}$2
+O2+O2$\stackrel{催化剂}{→}$2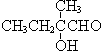 +2H2O,反应类型氧化反应
+2H2O,反应类型氧化反应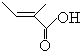 、
、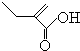 .
.