题目内容
17.取8g某有机物A,完全燃烧后只生成11gCO2和9gH2O.回答下列问题:(1)A分子中是(填:“是”或“不”)含氧元素.理由是(用数据说明)m(C)+m(H)=0.25mol×12g/mol+0.5mol×2×1g/mol=4g<8g.
(2)A 的实验式(最简式)为:CH4O.
(3)A的分子式能否确定?(填:“能”或“否”)能,理由是因为A的实验式中,C、H的组成已达饱和程度.
分析 根据元素守恒可知,有机物一定含有C、H元素,根据n=$\frac{m}{M}$计算有机物A、CO2、H2O的物质的量,根据质量守恒判断是否含有O元素,根据原子守恒计算有机物分子中含有各元素原子数目,确定有机物A的分子式,据此解答.
解答 解:(1)取8g某有机物A(相对分子质量为32)在氧气中完全燃烧,生成物中只有11g CO2和9g H2O,根据元素守恒可知,有机物一定含有C、H元素,
CO2的物质的量=$\frac{11g}{44g/mol}$=0.25mol,H2O的物质的量=$\frac{9g}{18g/mol}$=0.5mol,故m(C)+m(H)=0.25mol×12g/mol+0.5mol×2×1g/mol=4g<8g,故有机物A还含有O元素,故答案为:是;m(C)+m(H)=0.25mol×12g/mol+0.5mol×2×1g/mol=4g<8g;
(2)CO2的物质的量=$\frac{11g}{44g/mol}$=0.25mol,H2O的物质的量=$\frac{9g}{18g/mol}$=0.5mol,故m(C)+m(H)=0.25mol×12g/mol+0.5mol×2×1g/mol=4g,故有机物A还含有O元素,m(O)=8g-4g=4g,则n(O)=$\frac{4g}{16g/mol}$=0.25mol,
8g有机物A的物质的量=$\frac{8g}{32g/mol}$=0.25mol,有机物A中C原子数目=$\frac{0.25mol}{0.25mol}$=1、H原子数目=$\frac{0.5mol×2}{0.25mol}$4、O原子数目=$\frac{0.25mol}{0.25mol}$=1,故有机物的实验式(最简式)为CH4O,故答案为:CH4O;
(3)因为A的实验式中,C、H的组成已达饱和程度,所以实验式就是分子式,故答案为:能;因为A的实验式中,C、H的组成已达饱和程度.
点评 本题考查有机物分子式的确定,难度不大,注意利用质量守恒确定有机物中是否含有氧元素.

 阅读快车系列答案
阅读快车系列答案| A. | 乙烯和苯都能使溴水褪色,褪色的原因不相同 | |
| B. | 天然氨基酸能与强酸或强碱溶液反应 | |
| C. | 豆油、甘油、汽油都属于酯类 | |
| D. | 乙烯、苯、纤维素均属于烃类化合物 |
| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | KNO3晶体(NaCl),蒸馏水,结晶 | |
| D. | C2H5OH(水),加足量CaO,蒸馏 |
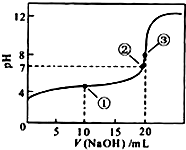 常温下,用0.1000mol•L-1NaOH溶液滴定 20.00mL0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1NaOH溶液滴定 20.00mL0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )| A. | 点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) | |
| B. | 点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(Na+)>c(OH-) |
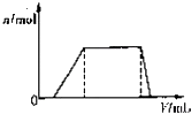 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、ClO-、AlO2- |
| A. | C、N、Si | B. | N、P、O | C. | N、O、S | D. | C、Si、S |
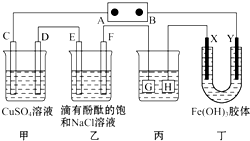 如图所示装置,C,D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极,将直流电源接通后,F极附近溶液呈红色.请回答:
如图所示装置,C,D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极,将直流电源接通后,F极附近溶液呈红色.请回答: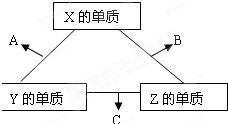
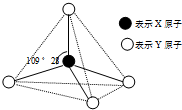 现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.请回答下列问题:
现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.请回答下列问题: