题目内容
5.下列说法中正确的是( )| A. | 氧化还原反应的本质是元素化合价的升降 | |
| B. | 氧化反应和还原反应必然同时发生 | |
| C. | 氧化反应是指反应中失去电子,所含元素化合价升高,被氧化 | |
| D. | 还原反应在反应中失去电子,所含元素化合价升高,被氧化 |
分析 A.氧化还原反应的本质为电子的转移;
B.氧化反应与还原反应同时发生;
C.还原剂失去电子发生氧化反应;
D.氧化剂得到电子发生还原反应.
解答 解:A.氧化还原反应的本质为电子的转移,特征为化合价的变化,故A错误;
B.氧化反应与还原反应同时发生,不存在先后反应的顺序,故B正确;
C.还原剂失去电子发生氧化反应,所含元素化合价升高,被氧化,故C正确;
D.氧化剂得到电子发生还原反应,所含元素化合价降低,被还原,故D错误;
故选BC.
点评 本题考查氧化还原反应,熟悉氧化还原反应中的基本概念即可解答,较简单,注重基础知识的考查.

练习册系列答案
相关题目
16.NaHCO3在日常生活和工农业生产中有重要用途,关于NaHCO3的说法不正确的是( )
| A. | 是一种钠盐 | B. | 是一种酸式盐 | C. | 水溶液显酸性 | D. | 是一种电解质 |
13.下列有关实验操作和现象描述的对应关系正确的是( )
| A. | 向AlCl3溶液中逐滴加入氨水,产生白色沉淀后消失 | |
| B. | 向Na2SiO3溶液中逐滴加入稀盐酸,产生白色胶状物 | |
| C. | 将NaOH溶液逐滴滴入FeSO4溶液中,只观察到白色沉淀 | |
| D. | 将砂纸打磨过的铝箔加热至熔化,熔化的铝以小液滴的形式滴落下来 |
10.下列反应在通常性情况下可以发生:①2FeCl3+Cu═2FeCl2+CuCl2;②Fe+CuSO4═FeSO4+Cu;③2FeCl3+2KI═2FeCl2+2KCl+I2;④6FeCl2+3Br2═4FeCl3+2FeBr2.则Br2,Fe3+,I2,Fe2+,Cu2+的氧化性强弱顺序是( )
| A. | Br2>Fe3+>I2 | B. | Fe3+>Br2>I2 | C. | Br2>I2>Fe3+ | D. | Fe3+>Cu2+>Fe2+ |
6.下列排列顺序不正确的是( )
| A. | 热稳定性:HF>HCl>HBr | B. | 碱性:Ca(OH)2>Mg(OH)2 | ||
| C. | 元素金属性:Na>Mg>Al | D. | 酸性:H3PO4>H2SO4>HClO4 |
3.短周期元素X、Y的原子序数相差2,下列有关叙述正确的是( )
| A. | X、Y不可能位于同一主族 | B. | X、Y一定位于同一周期 | ||
| C. | X、Y可能形成离子化合物XY | D. | X、Y不可能形成共价化合物XY2 |
4.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1L0.1mol•L-1的Na2SO4溶液中,含有Na+的个数为0.2NA | |
| B. | 常温常压下,11.2L氯气所含的氯原子数为NA | |
| C. | 14gN2的原子数为0.5NA | |
| D. | 1L0.1 mol•L-1CH3COOH溶液中含有0.1NA个H+ |
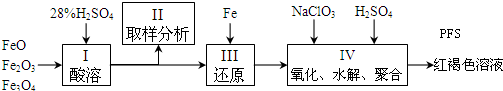
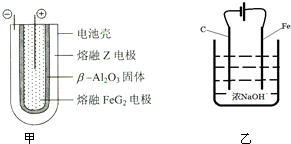 铝、铁是两种重要的金属元素,其单质及化合物在生产生活中的应用日趋广泛.
铝、铁是两种重要的金属元素,其单质及化合物在生产生活中的应用日趋广泛.