题目内容
6.下列排列顺序不正确的是( )| A. | 热稳定性:HF>HCl>HBr | B. | 碱性:Ca(OH)2>Mg(OH)2 | ||
| C. | 元素金属性:Na>Mg>Al | D. | 酸性:H3PO4>H2SO4>HClO4 |
分析 A、元素的非金属性越强,对应的氢化物越稳定;
B、元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
C、同一周期,原子序数越大,金属性越弱;
D、元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
解答 解:A.元素的非金属性:F>Cl>Br>I,元素的非金属性越强,对应的氢化物越稳定,则热稳定性:HI<HBr<HCl<HF,故A正确;
B.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故B正确;
C.Na、Mg、Al处于同一周期,随着原子序数的增大,金属性减弱,故C正确;
D.非金属性:Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性为H3PO4<H2SO4<HClO4,故D错误,
故选D.
点评 本题考查元素周期律的递变,题目难度不大,本题注意把握元素周期律的递变规律以及金属性、非金属性与最高价含氧酸、碱以及氢化物稳定性的关系.

练习册系列答案
相关题目
7.1mol•L-1 MgCl2溶液的含义是( )
| A. | 1L水中含有1 molMgCl2 | B. | 其中Cl-浓度为2 mol•L-1 | ||
| C. | 溶液中含有1 molMgCl2 | D. | 将95gMgCl2溶于1L水中所得的溶液 |
8.等质量的下列物质中,所含分子数最少的是( )
| A. | H2 | B. | HCl | C. | NH3 | D. | CH4 |
5.下列说法中正确的是( )
| A. | 氧化还原反应的本质是元素化合价的升降 | |
| B. | 氧化反应和还原反应必然同时发生 | |
| C. | 氧化反应是指反应中失去电子,所含元素化合价升高,被氧化 | |
| D. | 还原反应在反应中失去电子,所含元素化合价升高,被氧化 |
1.下列各组离子能在溶液中大量共存的是( )
| A. | HCO3-、Na+、OH-、K+ | B. | Cl-、NO3-、Fe2+、H+ | ||
| C. | Ba2+、OH-、Cl-、Na+ | D. | NH4+、Na+、NO3-、OH- |
11.往10mL 1mol/L AlCl3加入1mol/L NaOH溶液,得沉淀0.39g,则所加氢氧化钠溶液的体积可能为( )
| A. | 5 mL | B. | 25 mL | C. | 35 mL | D. | 45mL |
18.如表为元素周期表短周期的一部分.下列有关A、B、C、D、E 五种元素的叙述中正确的是( )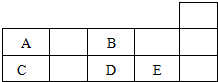

| A. | 对应阴离子的还原性:E>D | B. | 原子半径:C>B | ||
| C. | 对应氧化物的水化物的酸性:E>D | D. | A的非金属性弱于D |
15.下列有机物命名不正确的是( )
| A. | 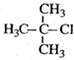 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | B. | 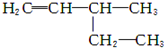 3-乙基-1-丁烯 3-乙基-1-丁烯 | ||
| C. | 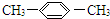 1,4-二甲苯 1,4-二甲苯 | D. | 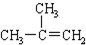 2-甲基丙烯 2-甲基丙烯 |