题目内容
13.下列有关实验操作和现象描述的对应关系正确的是( )| A. | 向AlCl3溶液中逐滴加入氨水,产生白色沉淀后消失 | |
| B. | 向Na2SiO3溶液中逐滴加入稀盐酸,产生白色胶状物 | |
| C. | 将NaOH溶液逐滴滴入FeSO4溶液中,只观察到白色沉淀 | |
| D. | 将砂纸打磨过的铝箔加热至熔化,熔化的铝以小液滴的形式滴落下来 |
分析 A、氢氧化铝不溶于过量氨水;
B、硅酸钠和盐酸反应生成硅酸白色沉淀;
C、氢氧化亚铁被空气中氧气氧化生成氢氧化铁;
D、铝在酒精灯上加热到熔化,生成熔点高的氧化铝,熔融但不滴落.
解答 解:A、向AlCl3溶液中逐滴加入氨水,产生白色沉淀氢氧化铝,不溶于氨水,故A错误;
B、向Na2SiO3溶液中逐滴加入稀盐酸反应生成硅酸,硅酸是白色胶状物,故B正确;
C、Fe(OH)2极不稳定,极易被空气中氧气氧化生成红褐色Fe(OH)3沉淀,所以看到的现象是:先生成白色沉淀,立即转化为灰绿色,最终转化为红褐色,故C错误;
D、铝在酒精灯上加热到熔化,因为表面有高熔点的氧化铝包着,所以不滴落,故D错误;
故选B.
点评 本题考查了物质性质的分析判断,反应产物、反应现象的分析注意物质反应过程中的特征现象应用,掌握基础是关键,题目较简单.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
3.下列有关说法正确的是( )
| A. | 陶瓷的主要成分是碳酸钙 | |
| B. | 用铁容器存放浓盐酸 | |
| C. | 硅是制造半导体的常用材料 | |
| D. | 工业上利用氨气制硝酸属于人工固氮 |
4.下列物质长期放置在空气中能发生氧化还原反应的是( )
| A. | Na2O2 | B. | Na2SO4 | C. | Na2CO3 | D. | NaOH |
1.下列有关实验装置进行的相应实验,能达到实验目的是( )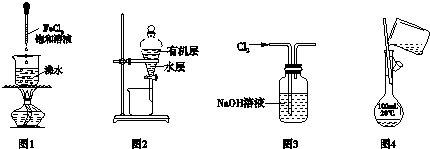

| A. | 用图1制备氢氧化铁胶体,当溶液至红褐色时继续煮沸 | |
| B. | 用图2所示装置分离CCl4萃取碘水后已分层的有机层和水层 | |
| C. | 用图3所示装置除去Cl2中含有的少量HCl气体 | |
| D. | 用图4所示装置配制实验所需100mL0.1mol/LNaCl溶液 |
8.等质量的下列物质中,所含分子数最少的是( )
| A. | H2 | B. | HCl | C. | NH3 | D. | CH4 |
18.下列叙述,正确的是( )
| A. | 电解质在电流的作用下发生电离 | |
| B. | 存在自由移动的离子是电解质溶液能导电的原因 | |
| C. | 金属铜能导电,所以铜是电解质 | |
| D. | 硫酸氢钠在水溶液中能电离出氢离子,所以硫酸氢钠属于酸 |
5.下列说法中正确的是( )
| A. | 氧化还原反应的本质是元素化合价的升降 | |
| B. | 氧化反应和还原反应必然同时发生 | |
| C. | 氧化反应是指反应中失去电子,所含元素化合价升高,被氧化 | |
| D. | 还原反应在反应中失去电子,所含元素化合价升高,被氧化 |
11.往10mL 1mol/L AlCl3加入1mol/L NaOH溶液,得沉淀0.39g,则所加氢氧化钠溶液的体积可能为( )
| A. | 5 mL | B. | 25 mL | C. | 35 mL | D. | 45mL |
12.下列说法正确的是( )
| A. | CH2Cl2与C2H4Br2均无同分异构体 | B. | C2H6与C3H8一定互为同系物 | ||
| C. | 在光照条件下乙烷能使氯水褪色 | D. | 烷烃在常温下均为气态 |