题目内容
某温度下 ,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示,据图分析,下列判断错误的是( )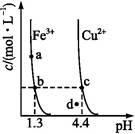
| A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
| B.加适量NH4Cl固体可使溶液由a点变到b点 |
| C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
| D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 |
B
解析

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将0.l mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
| A.溶液的pH增大 | B.CH3COOH电离的百分率变大 |
| C.溶液的导电能力减弱 | D.溶液中c(OH-)减小 |
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
对常温下pH=3的CH3COOH溶液,下列叙述不正确的是
| A.c(H+)=c(CHCOO-)+c(OH-) |
| B.加入少量CH3COONa固体后,c(CH3COO—)降低 |
| C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/L |
| D.与等体积pH =11的NaOH溶液混合后所得溶液显酸性 |
25 ℃时,在20 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )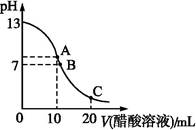
| A.在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| B.在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-) |
| C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
将0.1 mol下列物质置于1 L水中充分搅拌后,溶液中阴离子数最多的是( )
| A.KCl | B.Mg(OH)2 | C.Na2CO3 | D.MgSO4 |
下列事实不属于盐类水解应用的是( )
| A.明矾、氯化铁晶体常用于净水或消毒 |
| B.实验室通常使用热的纯碱溶液去除油污 |
| C.实验室配制FeCl3溶液时加入少量稀盐酸 |
| D.实验室制氢气时加入CuSO4可加快反应速率 |
下面是有关弱酸的电离平衡常数。
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 (25 ℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
结合数据,分析下列有关说法,其中错误的是( )
A.1 mol·L-1的溶液中,pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.升高温度,HCN溶液中H+浓度增大,平衡正向移动,电离平衡常数增大
C.向稀醋酸中逐滴加水,或加入少量冰醋酸,CH3COOH的电离平衡都正向移动
D.向CH3COOH溶液中加入少量氢氧化钠固体,平衡正向移动