题目内容
【题目】已知: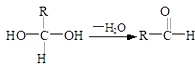
请根据下图回答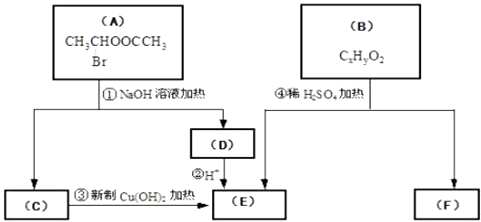
(1)E中含有的官能团的名称是;③的反应类型是 , C跟新制的氢氧化铜反应的化学方程式为: .
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1.则B的分子式为 , F的分子式为 .
(3)在电脑芯片生产领域,高分子光阻剂是光刻蚀0.11μm线宽芯片的关键技术.F是这种高分子光阻剂生产中的主要原料.F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③芳环上的一氯代物只有两种.F在一定条件下发生加聚反应的化学方程式为: .
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应.G可能有种结构,写出其中任意一种同分异构体的结构简式 .
【答案】
(1)羧基,氧化反应,CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O
CH3COOH+Cu2O↓+2H2O
(2)C10H10O2,C8H8O
(3)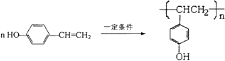
(4)4,![]() 或
或 ![]() (或间位、邻位任一种)
(或间位、邻位任一种)
【解析】解:(1)A在氢氧化钠水溶液、加热条件下发生水解反应C,根据A的结构中含有酯基、﹣Br,结合反应信息一个碳原子上连有两个羟基不稳定,转化为C=O,结合转化关系可推知C为CH3CHO,C与新制氢氧化铜反应生成E,故E为CH3COOH,含有的官能团名称是:羧基,反应③是乙醛发生氧化氧化反应生成乙酸,反应方程式为:CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O,
CH3COOH+Cu2O↓+2H2O,
所以答案是:羧基,氧化反应,CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O;
CH3COOH+Cu2O↓+2H2O;
(2)B在浓硫酸作用下生成乙酸与F,B应是酯,B的分子式为CxHyO2,相对分子质量为162,B分子中基团﹣CxHy的式量为162﹣32=130,故12x+y=13,所以 ![]() =10…10,故x的最大值为10,H原子数目为10,根据C原子与H原子的关系,x的值只能为10,故B的分子式为:C10H10O2,可推知F的分子式=C10H10O2+H2O﹣C2H4O2=C8H8O,
=10…10,故x的最大值为10,H原子数目为10,根据C原子与H原子的关系,x的值只能为10,故B的分子式为:C10H10O2,可推知F的分子式=C10H10O2+H2O﹣C2H4O2=C8H8O,
所以答案是:C10H10O2;C8H8O;
(3)F的相对分子质量为:162+18﹣60=120,F的结构中含有1个﹣OH,F能跟FeCl3溶液发生显色反应,说明含有苯环、酚羟基,决定为苯的二元取代,故剩余基团的相对分子质量为120﹣76﹣17=27,F能发生加聚反应,故还含有C=C,苯环上的一氯代物只有两种,说明为苯环二元对称取代,故F为 ![]() ,在一定条件下发生加聚反应生成高聚物,反应方程式为:
,在一定条件下发生加聚反应生成高聚物,反应方程式为:  ,
,
所以答案是:  ;
;
(4)化合物G是 ![]() 的同分异构体,它属于芳香族化合物,能发生银镜反应,说明含有苯环与醛基﹣CHO,若含有一个支链为﹣CH2CHO,只有1种结构,若有2个支链,则分别为﹣CH3、﹣CHO,2个支链有邻、间、对三种位置关系,有3种结构,故符合条件的化合物G的结构有1+3=4种,符合条件的同分异构体为:
的同分异构体,它属于芳香族化合物,能发生银镜反应,说明含有苯环与醛基﹣CHO,若含有一个支链为﹣CH2CHO,只有1种结构,若有2个支链,则分别为﹣CH3、﹣CHO,2个支链有邻、间、对三种位置关系,有3种结构,故符合条件的化合物G的结构有1+3=4种,符合条件的同分异构体为: ![]() 或
或 ![]() (或间位、邻位任一种),
(或间位、邻位任一种),
所以答案是:4; ![]() 或
或 ![]() (或间位、邻位任一种).
(或间位、邻位任一种).

 阅读快车系列答案
阅读快车系列答案