题目内容
17.下列叙述中正确的是( )| A. | H3O和OH-中具有相同的质子数和电子数 | |
| B. | 中子数为20的氯原子可表示为${\;}_{17}^{20}$Cl | |
| C. | 23592U 和23892U 是同位素,物理性质几乎相同,化学性质不同 | |
| D. | S2-的结构示意图 |
分析 A.一个氢氧根离子中的质子数是9个,电子数是10个;
B.原子符号中左上角的数字表示质量数;
C.互为同位素原子,核外电子排布相同,最外层电子数决定化学性质;
D.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8.
解答 解:A.H3O质子数为11,氢氧根离子中的质子数是9个,故A错误;
B.原子符号中左上角的数字表示质量数,质量数=质子数+中子数,则中子数为20的氯原子表示为3717Cl,故B错误;
C.互为同位素原子,核外电子排布相同,最外层电子数决定化学性质,同位素的化学性质几乎完全相同,但物理性质不同,故C错误;
D.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8;结构示意图 ,故D正确.
,故D正确.
故选D.
点评 本题考查化学用语、同位素等,明确质量数与质子数、中子数之间的相互关系,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
8.下列离子方程式书写正确的是( )
| A. | 石灰乳与Na2CO3溶液混合:Ca2++C${O}_{3}^{2-}$═CaCO3↓ | |
| B. | NH4HSO3溶液与足量NaOH溶液混合加热: N${H}_{4}^{+}$+HS${O}_{3}^{-}$+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+S${O}_{3}^{2-}$+2H2O | |
| C. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++S${O}_{4}^{2-}$+H++OH-═BaSO4↓+H2O |
2.下列说法正确的是( )
| A. | 电解饱和食盐水可制得金属钠 | |
| B. | 通过化学反应从海水中可提取氯化钠、溴、碘等物质 | |
| C. | 为了增强高锰酸钾溶液的氧化性可用盐酸酸化 | |
| D. | ClO2是一种有刺激性气味的黄绿色气体,除用于杀菌消毒外,还广泛用于环保、漂白、除臭 等方面 |
9.已知298K、101KPa条件下
2H2(g)+O2(g)=2H2O(g)△H1=-483.6kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
据此判断,下列说法正确的是( )
2H2(g)+O2(g)=2H2O(g)△H1=-483.6kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
据此判断,下列说法正确的是( )
| A. | H2(g)与O2(g)反应生成H2O(g)是吸热反应 | |
| B. | 1 molH2O(g)转变成1 molH2O(l)放出44.0kJ热量 | |
| C. | 1 molH2O(l)转变成1 molH2O(g)放出44.0kJ热量 | |
| D. | 1 molH2O(g)转变成1 molH2O(l)放出88.0kJ热量 |
6.以下关于混合物分离提纯操作或原理说法不正确的是( )
| A. | 实验室中用含有Ca2+、Mg2+、Cl-的自来水制取蒸馏水,可采用蒸馏的方法 | |
| B. | 用CCl4萃取碘水的实验中,振荡静置后,下层为紫红色溶液 | |
| C. | 利用植物油的密度比水小且不溶于水的原理,可用分液的方法分离这两种液体混合物 | |
| D. | 蒸馏时,温度计的水银球应充分接触溶液 |
7.下列离子方程式不正确的是( )
| A. | 在Ba(OH)2溶液中加入过量NaHCO3:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O | |
| B. | 硝酸银溶液与铜:Cu+2Ag+=Cu2++2Ag | |
| C. | 标准状况下2.24LCO2通入1mol/L50mLCa(OH)2溶液中:CO2+OH-=HCO3- | |
| D. | 金属铝溶于稀硫酸溶液:Al+2H+=Al3++H2↑ |
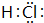 .
.