题目内容
12.除去括号内的杂质,写出除杂的试剂,并写出溶液中反应的离子方程式.(1)FeSO4(CuSO4)试剂Fe,离子方程式Fe+Cu2+═Fe2++Cu.
(2)CO2(HCl) 试剂饱和NaHCO3,离子方程式H++HCO3-═CO2↑+H2O.
(3)Cu(CuO)试剂HCl、硫酸皆可,离子方程式CuO+2H+═Cu2++H2O.
分析 (1)铁与硫酸铜反应生成硫酸亚铁和铜;
(2)氯化氢能够与碳酸氢钠反应生成二氧化碳、水和氯化钠,二氧化碳在饱和碳酸氢钠溶液中溶解度不大;
(3)氧化铜与稀硫酸或者盐酸反应生成可溶性酸盐,铜与稀硫酸或者盐酸酸不反应.
解答 解:(1)铁与硫酸铜反应生成硫酸亚铁和铜,可以选择Fe除去杂质,离子方程式:Fe+Cu2+═Fe2++Cu;
故答案为:Fe; Fe+Cu2+═Fe2++Cu;
(2)氯化氢能够与碳酸氢钠反应生成二氧化碳、水和氯化钠,二氧化碳在饱和碳酸氢钠溶液中溶解度不大,选择饱和碳酸氢钠溶液除去氯化氢杂质,离子方程式:H++HCO3-═CO2↑+H2O;
故答案为:饱和NaHCO3;H++HCO3-═CO2↑+H2O;
(3)氧化铜与稀硫酸或者盐酸反应生成可溶性酸盐,铜与稀硫酸或者盐酸酸不反应,选择盐酸或者稀硫酸除去杂质氧化铜,离子方程式:CuO+2H+═Cu2++H2O;
故答案为:HCl、硫酸皆可; CuO+2H+═Cu2++H2O.
点评 本题考查了物质的除杂和离子方程式的书写,明确物质性质及反应实质是解题关键,题目难度不大.

练习册系列答案
相关题目
2.有关有机物的燃烧下列说法正确的是( )
| A. | 可用点燃的方法鉴别甲烷,乙烯,丙烯和苯乙烯 | |
| B. | 1体积某气态烃完全燃烧生成的CO2比水蒸气少1体积(在相同条件下测定)可推知该烃为烷烃 | |
| C. | 等质量的乙醛和乙炔的耗氧量相同 | |
| D. | 任意比例混合的乙烯和1,3-丁二烯燃烧时只要总质量一定则生成的产物的质量也为定值 |
3.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1L 1mol/L 盐酸中含有HCl分子数为 1NA | |
| B. | 常温常压下,22.4L氧气所含的原子数为2NA | |
| C. | 实验室分别用KClO3和H2 O2制取3.2g O2时,转移的电子数均为0.4NA | |
| D. | 常温常压下,16 g 由O2和O3组成的混合气体所含电子数为8NA |
20.已知一种c(H+)=1×10-3 mol/L的一元酸溶液和一种c(OH-)=1×10-3mol/L的一元碱溶液等体积混合后溶液呈碱性,生成的盐可能是( )
| A. | 强酸强碱盐 | B. | 强酸弱碱盐 | ||
| C. | 强碱弱酸盐 | D. | 上述三种盐均可能 |
7.改变外界条件可以影响化学反应速率,针对H2(g)+I2(g)?2HI(g),其中能使活化分子百分数增加的是
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂( )
①增加反应物浓度 ②增大气体的压强 ③升高体系的温度 ④使用催化剂( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
17.下列叙述中正确的是( )
| A. | H3O和OH-中具有相同的质子数和电子数 | |
| B. | 中子数为20的氯原子可表示为${\;}_{17}^{20}$Cl | |
| C. | 23592U 和23892U 是同位素,物理性质几乎相同,化学性质不同 | |
| D. | S2-的结构示意图 |
1.分离和提纯下列混合物,将合理的方法填入下列空格内:
常见的物质分离和提纯的方法有:过滤,蒸发,升华,萃取,蒸馏,加热分解,结晶等.
| 序号 | 混合物 | 方法 |
| 1 | 海水中提取饮用水 | |
| 2 | 提取碘水中的碘 | |
| 3 | 从含少量氯化钠的硝酸钾溶液中提取硝酸钾 | |
| 4 | 从KNO3溶液中分离AgCl颗粒; | |
| 5 | 除去生石灰中混有少量的碳酸钙 |
2.下列变化中需加入氧化剂才能实现的是( )
| A. | H2SO4→BaSO4 | B. | Fe3+→Fe2+ | C. | CuO→Cu | D. | Fe→Fe2+ |
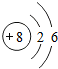 ;
;