题目内容
5.一定量的甲烷燃烧后得到CO、CO2及水蒸气,混合气共重49.6g,通过无水CaCl2时,CaCl2增重25.2g,则CO2的质量为( )| A. | 12.5 g | B. | 13.2 g | C. | 19.7 g | D. | 24.4 g |
分析 CH4燃烧产物为CO、CO2、H2O(g),产物通过无水CaCl2时,无水CaCl2的作用是吸收水分,无水CaCl2增重25.2g为水的质量,根据H原子守恒可计算CH4的物质的量,根据C原子守恒可计算CO和CO2的总的物质的量,再根据二者质量可计算CO2的物质的量,进而计算CO2质量.
解答 解:产物通过无水CaCl2时,无水CaCl2增重25.2g为水的质量,
所以n(H2O)=$\frac{25.2g}{18g/mol}$=1.4mol,
根据H原子守恒,可知:n(CH4)=$\frac{1}{2}$n(H2O)=$\frac{1}{2}$×1.4mol=0.7mol,
根据C原子守恒,则:n(CO)+n(CO2)=0.7mol,
所以m(CO)+m(CO2)=49.6g-25.2g=24.4g,
所以[0.7mol-n(CO2)]×28g/mol+n(CO2)×44g/mol=24.4g,
解之:n(CO2)=0.3mol,
所以生成二氧化碳的质量为0.3mol×44g/mol=13.2g.
故选:B.
点评 本题考查混合物的计算,难度中的,注意从原子守恒的角度解答,关键根据水的质量判断甲烷的物质的量.

练习册系列答案
相关题目
15.能一次区分乙酸、乙醇、苯三种物质的是( )
| A. | 水 | B. | 碳酸钠溶液 | C. | 溴水 | D. | 汽油 |
16.五倍子是一种常见的中草药,其有效成分为X.在一定条件下X可分别转化为Y、Z.下列说法错误的是( )
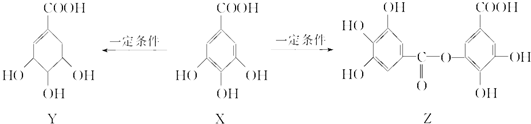

| A. | 1 mol X最多能与2 mol Br2发生取代反应 | |
| B. | Y分子结构中有3个手性碳原子 | |
| C. | 1 mol Z最多能与7 mol NaOH发生反应 | |
| D. | Y能发生加成、取代、消去、氧化、缩聚反应 |
20.含手性碳原子的分子称手性分子,手性分子具有光学活性.如下图有机物具有光学活性(式中标有*号的为手性碳原子),该有机物发生下列哪种反应后,产生物仍然一定具有光学活性( )
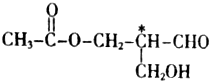
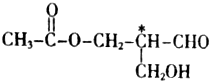
| A. | 银镜反应 | B. | 水解反应 | C. | 消去反应 | D. | 酯化反应 |
10.下列各组分子中,都属于含极性键的非极性分子的是( )
| A. | C2H4 CH4 | B. | CO2 H2S | C. | C60 C2H4 | D. | NH3 HCl |
17.某有机物的结构简式如下所示,该有机物可能具有的性质是( )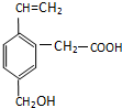
①可以燃烧
②能使酸性KMnO4溶液褪色
③能跟NaOH溶液反应
④能发生酯化反应
⑤能发生加成反应.

①可以燃烧
②能使酸性KMnO4溶液褪色
③能跟NaOH溶液反应
④能发生酯化反应
⑤能发生加成反应.
| A. | 只有②③④ | B. | 只有①②③④ | C. | ①②③④⑤ | D. | 只有②④ |
14.下列关于如图所示原电池装置的叙述中,正确的是( )
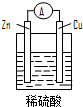

| A. | 铜片是负极 | B. | 铜片表面反应为:Cu-2e- Cu2+ | ||
| C. | 电流从锌片经导线流向铜片 | D. | 氢离子在铜片表面被还原 |
15.下列说法中正确的是( )
| A. | 金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动 | |
| B. | 金属晶体的熔点和沸点都很高 | |
| C. | 金属元素和非金属元素形成的化合物一定是离子化合物 | |
| D. | 离子化合物中一定含有离子键 |
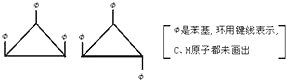 1,2,3-三苯基环丙烷的3个苯基可以分布在环丙环平面的上下,因此有如下2个异构体.[Φ是苯基,环用键线表示,C、H原子都未画出]据此,可判断1,2,3,4,5-五氯环戊烷(假定五个碳原子也处于同一平面上)的异构体数是( )
1,2,3-三苯基环丙烷的3个苯基可以分布在环丙环平面的上下,因此有如下2个异构体.[Φ是苯基,环用键线表示,C、H原子都未画出]据此,可判断1,2,3,4,5-五氯环戊烷(假定五个碳原子也处于同一平面上)的异构体数是( )