题目内容
14.下列关于如图所示原电池装置的叙述中,正确的是( )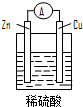
| A. | 铜片是负极 | B. | 铜片表面反应为:Cu-2e- Cu2+ | ||
| C. | 电流从锌片经导线流向铜片 | D. | 氢离子在铜片表面被还原 |
分析 A、原电池中一般是活泼金属做负极;
B、原电池的正极是析出金属或者是析出气体;
D、原电池中电流和电子流向相反,即电流从正极流向负极;
D、只有原电池的正极可能会是氢离子被还原生成气体;
解答 解:A、Zn、Cu、硫酸构成的原电池中,活泼金属锌做负极,金属铜做正极,故A错误;
B、原电池的正极Cu片极上的反应是:2H++2e-→H2↑,故B错误;
C、原电池中电流从正极流向负极,即从铜片经导线流向锌片,故C错误;
D、该原电池的正极反应是:2H++2e-→H2↑,氢离子在铜片表面被还原,故D正确.
故选D.
点评 本题考查学生原电池的工作原理,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
4.在含有NaI、Na2SO3和FeBr2各1mol的溶液中通入足量的Cl2,将溶液在空气中加热蒸干并充分灼烧,最终得到剩余的固体物质是( )
| A. | NaCl、FeCl3、Na2SO4、I2 | B. | NaCl、FeBr3、Na2SO4 | ||
| C. | NaCl、Fe2O3、Na2SO4 | D. | NaBr、FeCl3 |
5.一定量的甲烷燃烧后得到CO、CO2及水蒸气,混合气共重49.6g,通过无水CaCl2时,CaCl2增重25.2g,则CO2的质量为( )
| A. | 12.5 g | B. | 13.2 g | C. | 19.7 g | D. | 24.4 g |
2.下列叙述正确的是( )
| A. | 硫酸钡的水溶液几乎不导电,所以硫酸钡是弱电解质 | |
| B. | 二氧化硫和二氧化氮的水溶液都能导电,所以二者都是电解质 | |
| C. | 氨气的水溶液可以导电,所以氨是电解质 | |
| D. | 氢氧化钙在水中的溶解度很小,但它溶解的部分完全电离,所以氢氧化钙是强电解质 |
9.在由5种基团-CH3、-OH、-CHO、-C6H5、-COOH两两组成的物质中,能与NaOH反应的有机物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
6.下列有机物的命名正确的是( )
| A. | CH3CH2C(CH3)2CH(C2H5)CH3:2-乙基-3,3-二甲基戊烷 | |
| B. | HC≡C-CH2CH(CH3)-CH3:2-甲基-5-戊炔 | |
| C. | CH3CHClCH2CHClCH2CH2Cl:2,4,6-三氯己烷 | |
| D. | CH3CHOHCH2CHOHCHOHCH3:2,3,5-己三醇 |
4.某乙醇水溶液的质量分数为w%,物质的量浓度为cmol/L,密度为dg/mL,1Kg这种溶液中含有的乙醇是( )
| A. | 46C | B. | $\frac{c}{d}$mol | C. | c mol | D. | 1000dw g |
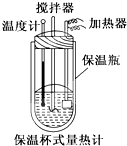 已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.请回答下列问题:
已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.请回答下列问题: