题目内容
18.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )| 物质 | 试剂 | 分离方法 | |
| ① | 甲烷(乙烯) | 高锰酸钾溶液 | 洗气 |
| ② | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(苯酚) | 浓溴水 | 过滤 |
| A. | ②③ | B. | ①③ | C. | ①② | D. | ①④ |
分析 ①乙烯易被酸性高锰酸钾溶液氧化生成二氧化碳;
②溴和氢氧化钠反应生成溴化钠、次溴酸钠,溴苯和氢氧化钠溶液不反应;
③生石灰与水反应,乙醇易挥发;
④苯酚和溴水反应生成的三溴苯酚易溶于苯.
解答 解:①乙烯易被酸性高锰酸钾溶液氧化生成二氧化碳,引进新的杂质,乙烯和溴水反应、甲烷和溴水不反应,所以可以用溴水做除杂剂,采用洗气方法分离,故错误;
②溴和氢氧化钠反应生成溴化钠、次溴酸钠,溴苯和氢氧化钠溶液不反应,溶液分层,然后采用分液方法分离,故正确;
③乙醇与水的沸点不同,且生石灰与水反应,可用蒸馏的方法分离,故正确;
④苯酚和溴水反应生成的三溴苯酚易溶于苯,苯酚易溶于氢氧化钠溶液、苯不易溶于氢氧化钠溶液,然后采用分液方法分离,故错误;
故选A.
点评 本题考查物质分离和提纯,为高频考查,侧重考查基本理论,明确物质性质的差异性是解本题关键,注意除杂时不能引进新的杂质,难点是除杂剂的选取,题目难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
8.在25℃时,用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
| A. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | B. | $\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ | ||
| C. | $\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ | D. | $\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$、 |
6.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有( )
| A. | 12g金刚石中含4NA个C-C共价键 | |
| B. | 2L 0.5 moI.L-1盐酸溶液所含的HCI分子数目为NA | |
| C. | 标准状况下,2.24LCL4含有的原子数为0.5NA | |
| D. | 7.1 gCL2与5.6 g Fe反应,转移的电子总数为0,2NA |
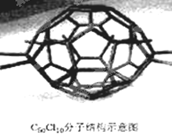
13.厦门大学郑兰荪院士合成了C70Cl10富勒烯足球状分子,如图,它是由C70分子与Cl2发生加成反应得到的.在C70分子中每个碳原子均与周围相邻的其他3个碳原子相连,70个碳原子组成若干个正六边形和正五边形.则有关说法中不正确的是
( )
( )

| A. | C70的熔点比石墨的熔点低 | |
| B. | C70和金刚石是同素异形体 | |
| C. | C70分子中含有70个σ键,35个π键 | |
| D. | C70Cl10分子中共用电子对数目为145个 |
3.如图表示从混合物中分离出X的两种方案,根据方案I和方案Ⅱ下列说法合理的是( )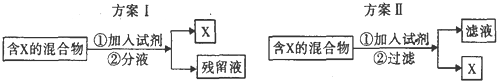

| A. | 若含X的混合物为碘水,可通过方案I进行分离,加入试剂为CC14液体,充分振荡后液体分层,上层为X的CC14溶液 | |
| B. | 若含X的混合物为乙醇和水,可通过方案Ⅱ进行分离,加入试剂为生石灰 | |
| C. | 若含X的混和物为KNO3和NaCl,可通过方案II进行分离,加入试剂为适量沸水 | |
| D. | 若含X的混合物为皂化反应后的混合物,可通过方案I进行分离,加入试剂为饱和食盐水,残留液中含有甘油 |
10.在反应2SO2+18O2?2SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
| A. | SO2 | B. | O2 SO3 | C. | SO2 O2 SO3 | D. | SO2 SO3 |
7.下列物质久置空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A. | 澄清的石灰水变浑浊 | B. | 浓硫酸的质量增重 | ||
| C. | 氢氧化钠的表面发生潮解 | D. | 铝的表面生成致密的薄膜 |