题目内容
【题目】对工业废水和生活污水进行处理是防止水体污染的主要措施.
![]() 水的净化和软化的区别是 ______
水的净化和软化的区别是 ______
![]() 在实验室中过滤操作需要用到的玻璃仪器有 ______ .
在实验室中过滤操作需要用到的玻璃仪器有 ______ .
![]() 下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 ______
下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是 ______ ![]() 填字母
填字母![]() .
.
![]() 福尔马林
福尔马林![]() 漂白粉
漂白粉![]() 臭氧
臭氧![]() 氯气
氯气
![]() 是一种新型水处理剂,工业上可用
是一种新型水处理剂,工业上可用![]() 制备
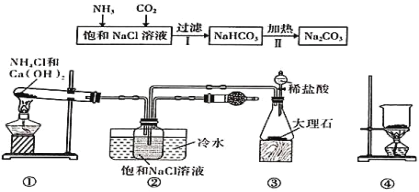
制备![]() 其工艺流程如图:
其工艺流程如图:
![]()
![]() 工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因 ______
工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾.请解释这一做法的原因 ______ ![]() 用必要的离子方程式和文字描述
用必要的离子方程式和文字描述![]() .
.
![]() 假设每步反应均是完全的,若制取3molNa2FeO4,需要NaClO固体 ______
假设每步反应均是完全的,若制取3molNa2FeO4,需要NaClO固体 ______ ![]()
![]() 写出第一步在酸性环境下加入H2O2的离子反应方程式 ______ .
写出第一步在酸性环境下加入H2O2的离子反应方程式 ______ .
![]() 石灰纯碱法是常用的硬水软化方法,已知
石灰纯碱法是常用的硬水软化方法,已知![]() 时
时![]() ,现将等体积的
,现将等体积的![]() 溶液与
溶液与![]() 溶液混合
溶液混合![]() 假设溶液体积具有加和性
假设溶液体积具有加和性![]() ,若
,若![]() 溶液的浓度为
溶液的浓度为![]() ,则生成沉淀所需Ca(OH)2溶液的最小浓度为 ______ .
,则生成沉淀所需Ca(OH)2溶液的最小浓度为 ______ .
【答案】水的净化是除去悬浮物和污染物,而水的软化是除去水中较多的钙离子和镁离子 玻璃棒、烧杯、普通漏斗![]() 胶头滴管
胶头滴管![]() c
c ![]() 在碱性条件下易被氧化成
在碱性条件下易被氧化成![]() ,进而水解生成
,进而水解生成![]() 胶体,起到较好的混凝作用,
胶体,起到较好的混凝作用,![]() 胶体
胶体![]()
![]()
![]()
![]()
【解析】
![]() 根据水的净化和软化的本质来分析;
根据水的净化和软化的本质来分析;
![]() 过滤除去溶液中的不溶性杂质的方法,根据过滤装置来分析;
过滤除去溶液中的不溶性杂质的方法,根据过滤装置来分析;
![]() 对自来水进行杀菌消毒,且不会造成二次污染,只有臭氧的还原产物对水无污染;
对自来水进行杀菌消毒,且不会造成二次污染,只有臭氧的还原产物对水无污染;
![]() 将待处理水的pH调到9左右,再加入绿矾,可得到铁离子,水解生成胶体;
将待处理水的pH调到9左右,再加入绿矾,可得到铁离子,水解生成胶体;
![]() 发生氧化还原反应生成
发生氧化还原反应生成![]() ;
;
③H2O2在酸性条件下能将![]() 氧化为
氧化为![]() ,H2O2被还原为水,据此写出离子方程式;
,H2O2被还原为水,据此写出离子方程式;
![]() 溶液的浓度为
溶液的浓度为![]() ,等体积混合后溶液中
,等体积混合后溶液中![]() ,根据
,根据![]() 计算沉淀时混合溶液中
计算沉淀时混合溶液中![]() ,以此来解答.
,以此来解答.
解:![]() 水的净化即水的除杂,除去水中的杂质;水的软化是将硬水转化为软水,降低钙离子和镁离子,
水的净化即水的除杂,除去水中的杂质;水的软化是将硬水转化为软水,降低钙离子和镁离子,
故答案为:水的净化是除去悬浮物和污染物,而水的软化是除去水中较多的钙离子和镁离子;
![]() 过滤除去溶液中的不溶性杂质的方法,使用的玻璃仪器有玻璃棒、烧杯、普通漏斗
过滤除去溶液中的不溶性杂质的方法,使用的玻璃仪器有玻璃棒、烧杯、普通漏斗![]() 胶头滴管
胶头滴管![]() ,故答案为:玻璃棒、烧杯、普通漏斗
,故答案为:玻璃棒、烧杯、普通漏斗![]() 胶头滴管
胶头滴管![]() ;
;
![]() 福尔马林有毒,含氯物质可导致二次污染,则能够用来对自来水进行杀菌消毒,且不会造成二次污染的只有臭氧,故答案为:c;
福尔马林有毒,含氯物质可导致二次污染,则能够用来对自来水进行杀菌消毒,且不会造成二次污染的只有臭氧,故答案为:c;
![]() 工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加绿矾,原因:
工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加绿矾,原因:![]() 在碱性条件下易被氧化成
在碱性条件下易被氧化成![]() ,进而水解生成
,进而水解生成![]() 胶体,起到较好的混凝作用,
胶体,起到较好的混凝作用,![]() 胶体
胶体![]() ,
,
故答案为:![]() 在碱性条件下易被氧化成
在碱性条件下易被氧化成![]() ,进而水解生成
,进而水解生成![]() 胶体,起到较好的混凝作用,
胶体,起到较好的混凝作用,![]() 胶体
胶体![]() ;
;
![]() 由Fe(OH)3制取
由Fe(OH)3制取![]() 的化学方程式为:
的化学方程式为:![]() ,设需要的NaClO的物质的量为Xmol,
,设需要的NaClO的物质的量为Xmol,
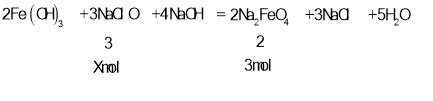
解得![]()
则NaClO的质量![]()
故答案为:![]() ;
;
③H2O2在酸性条件下能将![]() 氧化为
氧化为![]() ,H2O2被还原为水,故离子方程式为:
,H2O2被还原为水,故离子方程式为:![]() ,
,
故答案为:![]() ;
;
![]() 溶液的浓度为
溶液的浓度为![]() ,等体积混合后溶液中
,等体积混合后溶液中![]() ,根据
,根据![]() 可知,
可知,![]() ,原溶液
,原溶液![]() 溶液的最小浓度为混合溶液中
溶液的最小浓度为混合溶液中![]() 的2倍,故原溶液
的2倍,故原溶液![]() 溶液的最小浓度为
溶液的最小浓度为![]() ,故答案为:
,故答案为:![]() .
.

 53天天练系列答案
53天天练系列答案