题目内容
【题目】下图是与乙醇有关的两个实验,
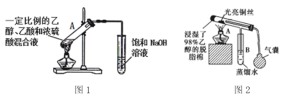
(1)图1试管A中的反应方程式为______________________________。请指出图1中两处明显的错误①________________________________;②_________________________________。
(2)点燃图2中酒精灯,反复挤压气囊,向图2装置中鼓入空气,铜丝反复出现由红变黑又由黑变红的现象,请写出相应的化学反应方程式____________________、____________________在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是________(填“吸热”或“放热”)反应。
(3)图2反应进行一段时间后,若试管B中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有__________(填名称)。要除去该物质,可先在混合液中加入_____(填写字母),
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________________(填实验操作名称)即可除去。
【答案】CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O 导管末端伸入液面以下,易造成倒吸 饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率 2Cu+O2
CH3COOCH2CH3+H2O 导管末端伸入液面以下,易造成倒吸 饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率 2Cu+O2![]() 2CuO CH3CH2OH+CuO
2CuO CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 放热 乙酸 c 蒸馏
CH3CHO+Cu+H2O 放热 乙酸 c 蒸馏
【解析】
图1为乙酸乙酯的制备实验,乙醇、乙酸和浓硫酸的混合液共热,反应生成乙酸乙酯,试管中盛放饱和碳酸钠溶液,可降低乙酸乙酯的溶解度,同时反应挥发出的乙酸,溶解乙醇,便于溶液分层,为防止倒吸,导管不能插入液面以下;图2为乙醇的催化氧化实验,加热条件下,铜先和氧气反应生成氧化铜,挥发的乙醇在加热条件被氧化铜氧化成乙醛,铜丝反复出现由红变黑又由黑变红的现象。
(1)乙酸和乙醇的酯化反应方程式为CH3COOH+HOCH2CH3![]() CH3COOCH2CH3+H2O;根据分析图示错误为:导管末端伸入液面以下,易造成倒吸;乙酸乙酯在碱性环境下发生水解,所以饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率;
CH3COOCH2CH3+H2O;根据分析图示错误为:导管末端伸入液面以下,易造成倒吸;乙酸乙酯在碱性环境下发生水解,所以饱和NaOH溶液碱性太强,易造成乙酸乙酯水解而降低产率;
(2)铜丝反复出现由红变黑又由黑变红的现象,说明铜先和氧气反应生成氧化铜,挥发的乙醇在加热条件被氧化铜氧化成乙醛,氧化铜被还原为铜,反应的方程式为2Cu+O2![]() 2CuO、CH3CH2OH+CuO
2CuO、CH3CH2OH+CuO![]() CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是放热反应;
CH3CHO+Cu+H2O;熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是放热反应;
(3)若试管B中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体显酸性,根据各物质的性质可以应是乙醛被氧化生成的乙酸;乙酸可以和碳酸氢钠溶液反应生成盐,增大与乙醇、乙醛的熔沸点差异,所以之后再进行蒸馏分离即可。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案