题目内容
下列说法不正确的是( )
| A、漂白粉长时间露置空气中会变质失效 |
| B、澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液 |
| C、高温下SiO2能与Na2CO3反应放出CO2,但不能说明H2SiO3的酸性强于H2CO3 |
| D、金属的化学腐蚀和电化学腐蚀的本质相同,但电化学腐蚀伴有电流产生 |
考点:氯、溴、碘及其化合物的综合应用,金属的电化学腐蚀与防护,硅和二氧化硅,钠的重要化合物
专题:元素及其化合物
分析:A.漂白粉长时间露置空气中,与二氧化碳、水反应生成HClO,且HClO不稳定;
B.Na2CO3和NaHCO3溶液与石灰水反应均生成白色沉淀;
C.利用溶液中的强酸制取弱酸的反应比较酸性;
D.金属的化学腐蚀和电化学腐蚀的实质均为金属失去电子的过程,但电化学腐蚀中有原电池反应.
B.Na2CO3和NaHCO3溶液与石灰水反应均生成白色沉淀;
C.利用溶液中的强酸制取弱酸的反应比较酸性;
D.金属的化学腐蚀和电化学腐蚀的实质均为金属失去电子的过程,但电化学腐蚀中有原电池反应.
解答:
解:A.漂白粉长时间露置空气中,与二氧化碳、水反应生成HClO,且HClO不稳定,则漂白粉变质会失去漂白效果,故A正确;
B.Na2CO3和NaHCO3溶液与石灰水反应均生成白色沉淀,现象相同,不能鉴别,故B错误;
C.利用溶液中的强酸制取弱酸的反应比较酸性,则高温下SiO2能与Na2CO3反应放出CO2,不能说明H2SiO3的酸性强于H2CO3,故C正确;
D.金属的化学腐蚀和电化学腐蚀的实质均为金属失去电子的过程,但电化学腐蚀中有原电池反应,伴随电流产生,而化学腐蚀不存在,故D正确;
故选B.
B.Na2CO3和NaHCO3溶液与石灰水反应均生成白色沉淀,现象相同,不能鉴别,故B错误;
C.利用溶液中的强酸制取弱酸的反应比较酸性,则高温下SiO2能与Na2CO3反应放出CO2,不能说明H2SiO3的酸性强于H2CO3,故C正确;
D.金属的化学腐蚀和电化学腐蚀的实质均为金属失去电子的过程,但电化学腐蚀中有原电池反应,伴随电流产生,而化学腐蚀不存在,故D正确;
故选B.
点评:本题考查较综合,综合考查元素化合物知识,为高频考点,涉及物质的性质、物质的鉴别、酸性比较及金属腐蚀等,注重常考考点的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
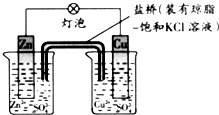 铜锌原电池工作时,下列叙述正确的是( )
铜锌原电池工作时,下列叙述正确的是( )| A、正极反应为:Zn-2e-=Zn2+ |
| B、在外电路中,电子从铜片流向锌片 |
| C、电池反应为:Zn+Cu2+=Zn2++Cu |
| D、盐桥中的K+移向ZnSO4溶液 |
在100mL 1.0mol/L的AlCl3溶液中加入350mL 1.0mol/L的NaOH溶液充分反应后,得到的沉淀的质量是( )
| A、7.8g | B、3.9g |
| C、15.6g | D、无沉淀 |
下列各组离子在给定条件下能大量共存的是( )
| A、能使pH试纸呈红色的溶液:Na+、NH4+、Cl-、NO3- |
| B、滴入KSCN溶液显血红色的溶液:K+、Na+、CO32-、I- |
| C、能与铝反应产生H2的溶液:K+、Fe2+、Cl-、NO3- |
| D、常温下由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl- |
某元素原子核外的电子排布式为1s2…(n-1)d10ns2np2,下列对该元素的判断错误的是( )
| A、一定不是短周期元素 |
| B、可能属于过渡元素 |
| C、一定位于元素周期表的第14列上 |
| D、一定不是非金属元素 |
下列相关表达正确的是( )
| A、亚硫酸的电离方程式:H2SO3=2H++SO2-3 | ||
B、中子数为18的氯原子的原子符号:
| ||
| C、(CH3)2CHCH2CH2OH的名称:3-甲基-1-丁醇 | ||
D、HOCH2COOH缩聚产物的结构简式: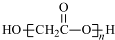 |
 (1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O.已知室温下2g SiH4自燃放出热量89.2kJ.SiH4自燃的热化学方程式为