题目内容
下列有关物质性质的应用正确的是( )
| A、氧化铝熔点很高,可制造用于熔融烧碱的坩埚 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 |
| D、SO2具有漂白性,可用作熏蒸粉丝使其增白 |
考点:硅和二氧化硅,二氧化硫的化学性质,镁、铝的重要化合物
专题:氧族元素,碳族元素,几种重要的金属及其化合物
分析:A.氧化铝为两性氧化物,能够与氢氧化钠发生反应;
B.高温条件下碳与二氧化硅反应生成一氧化碳和硅;
C.二氧化硅与氢氟酸在常温下反应生成四氟化硅;
D.二氧化硫有毒,不能用于食品添加剂.
B.高温条件下碳与二氧化硅反应生成一氧化碳和硅;
C.二氧化硅与氢氟酸在常温下反应生成四氟化硅;
D.二氧化硫有毒,不能用于食品添加剂.
解答:
解:A.氧化铝与氢氧化钠反应:Al2O3+2NaOH=2NaAlO2+H2O,故A错误;
B.炭具有还原性,一定条件下能将二氧化硅还原为硅,方程式为:SiO2+2 C
Si+2 CO↑,故B正确;
C.二氧化硅与氢氟酸在常温下反应的化学方程式为:4HF+SiO2=SiF4+2H2O 故C错误;
D.二氧化硫有毒,不能用于食品添加剂,故D错误;
故选:B.
B.炭具有还原性,一定条件下能将二氧化硅还原为硅,方程式为:SiO2+2 C
| ||
C.二氧化硅与氢氟酸在常温下反应的化学方程式为:4HF+SiO2=SiF4+2H2O 故C错误;
D.二氧化硫有毒,不能用于食品添加剂,故D错误;
故选:B.
点评:本题考查了常见物质的性质,题目难度不大,明确二氧化硅、二氧化硫、氧化铝的性质是解题关键,注意二氧化硅常温下就能与氢氟酸反应,所以保存氢氟酸不能用玻璃瓶,可以塑料瓶.

练习册系列答案
相关题目
1L的密闭容器中有0.3mol A、0.1mol C和一定量B三种气体.一定条件下发生反应,各物质浓度随时间变化如图甲所示,t1时刻c(B)=0.1mol/L.图乙为t2时刻后改变条件反应速率随时间的变化情况,每次改变一种条件且条件各不相同,已知,t3时刻为加入催化剂,则下列判断正确的是( )
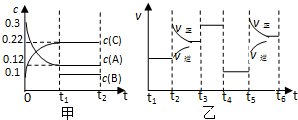

| A、t4时刻是增大容器的体积 |
| B、B的起始浓度为0.06mol/L |
| C、t1、t3、t6时刻相比,A物质的量最大的是t6时刻 |
| D、该可逆反应的方程式为:3A(g)?B(g)+2C(g) |
下列与有机物的结构、性质、用途有关的叙述,不正确的是( )
| A、乙醇、乙酸、乙酸乙酯都能发生取代反应 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| C、乙烯和聚乙烯中均含有不饱和碳碳双键 |
| D、淀粉和蛋白质都是高分子化合物 |
下列说法不正确的是( )
| A、无热效应的自发过程是不存在的 |
| B、冰融化过程其熵值增加 |
| C、铁生锈、氢气燃烧均为自发放热过程 |
| D、同一物质固态时熵值最小 |
铅蓄电池是可充电型电池,电池总反应为:Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列说法正确的是( )
| 放电 |
| 充电 |
| A、该蓄电池放电工作时SO42-向正极移动 |
| B、充电时阳极的电极反应式是Pb+SO42--2e-═PbSO4 |
| C、用铅蓄电池电解氯化钠溶液,当阳极上收集到11.2L氯气时(标况下),理论上负极板的质量增加48g |
| D、铅蓄电池为电解电源,当蓄电池中有0.4mol H+被消耗时,电路中通过的电子的物质的量为0.4mol |
乙醇与乙酸在一定条件下反应生成乙酸乙酯,该反应类型属于( )
| A、加成反应 | B、酯化反应 |
| C、置换反应 | D、复分解反应 |
某有机物的结构为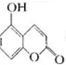 ,下列有关说法正确的是( )
,下列有关说法正确的是( )
 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A、1mol该物质与足量浓溴水反应,最多消耗2mol Br2 |
| B、1mol该物质最多能与2mol NaOH反应 |
| C、1mol该物质最多能与3mol H2加成 |
| D、该物质的核磁共振氢谱共有6个吸收峰 |
1L 0.2mol/L的KI溶液中,含溶质KI的物质的量是( )
| A、0.2 mol |
| B、0.5 mol |
| C、2 mol |
| D、5 mol |
金刚石与石墨是碳的两种同素异形体,在100kPa时,1mol石墨转化为金刚石要吸收1.895kJ的热量,下列说法正确的是( )
| A、金刚石比石墨稳定 |
| B、1mol石墨比1mol金刚石的总能量低 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、石墨比金刚石稳定 |