题目内容
乙醇与乙酸在一定条件下反应生成乙酸乙酯,该反应类型属于( )
| A、加成反应 | B、酯化反应 |
| C、置换反应 | D、复分解反应 |
考点:有机化学反应的综合应用
专题:有机反应
分析:乙酸与乙醇反应生成乙酸乙酯和水,反应的方程式为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,该反应为酯化反应,也属于取代反应,据此进行解答.
| 浓硫酸 |
| △ |
解答:
解:乙醇与乙酸在一定条件下反应生成乙酸乙酯:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,该反应属于有机反应中的酯化反应,酯化反应也属于取代反应,
故选B.
| 浓硫酸 |
| △ |
故选B.
点评:本题考查了化学应类型的判断,题目难度不大,注意常见反应类型及判断方法,明确加成反应、取代反应、酯化反应等反应的原理及区别.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
| A、2.24L C4H6中含有碳碳叁键数一定为0.1×6.02×1023 |
| B、在标准状态下,11.2L NO与11.2L O2混合后气体分子数为0.75NA |
| C、含1mol FeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA |
| D、106g Na2CO3固体中的阴离子数为NA |
过氧化钠跟足量的NaHCO3混合后,在密闭容器中充分加热,排除气体物质后冷却残留的固体物质是( )
| A、Na2O2、Na2CO3 |
| B、NaOH、Na2CO3 |
| C、Na2CO3 |
| D、Na2O2、NaOH、Na2CO3 |
从化学角度分析,下列叙述不正确的是( )
| A、化学是以实验为基础的一门学科,定量研究方法是化学发展为一门学科的重要标志 |
| B、铝表面有一层致密的氧化物薄膜,故铝制容器可用来腌制咸菜等 |
| C、明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的净化 |
| D、高空中臭氧层能够吸收太阳紫外线,为地球上的生物提供了天然的保护屏障.但低空的臭氧是污染气体,会给人体造成伤害 |
下列有关物质性质的应用正确的是( )
| A、氧化铝熔点很高,可制造用于熔融烧碱的坩埚 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 |
| D、SO2具有漂白性,可用作熏蒸粉丝使其增白 |
元素X、Y、Z原子序数之和为33,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A、在短周期元素中X的金属性最强 |
| B、Y的最高价含氧酸属于弱酸 |
| C、原子半径Z>Y,离子半径Z2->X+ |
| D、Y、Z都可与氢元素形成氢化物,Z的氢化物比Y的氢化物稳定 |
如图是一种原电池装置,关于该装置工作时的叙述错误的是( )


| A、锌作负极 |
| B、铜片上有气泡产生 |
| C、将电能转化为化学能 |
| D、锌片的电极反应式为:Zn-2e-=Zn2+ |
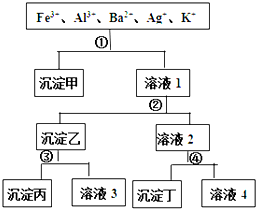 某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3?H2O、NaCl四种溶液,按如图所示的步骤分开五种离子.下列判断正确的是( )
某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3?H2O、NaCl四种溶液,按如图所示的步骤分开五种离子.下列判断正确的是( )| A、沉淀乙是氢氧化铝和氢氧化银的混合物 |
| B、溶液3中含有Al3+ |
| C、溶液4含有三种阳离子,分别是H+、Na+、K+ |
| D、试剂①是NaCl,试剂④是H2SO4 |