题目内容
【题目】现有部分短周期元素的原子结构如下表:
元素编号 | 元素原子结构 |
X | 原子结构示意图为 |
Y | 最外层电子数是次外层电子数的2倍 |
Z | 原子核内含有12个中子,且其离子的结构示意图为 |
(1)写出X的元素符号:____________,元素Y的最简单氢化物的化学式为______________。
(2)Z元素原子的相对原子质量为____________。
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为______________。
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式为__________________。
【答案】N CH4 23 H++OH-=H2O 2CO2+2Na2O2=2Na2CO3+O2
【解析】
由 X原子结构示意图为![]() 可知,a=7,质子数为7的元素为氮;由Y元素最外层电子数是次外层电子数的2倍,所以Y元素为碳元素;由Z的原子核内含有12个中子,且其离子的结构示意图为
可知,a=7,质子数为7的元素为氮;由Y元素最外层电子数是次外层电子数的2倍,所以Y元素为碳元素;由Z的原子核内含有12个中子,且其离子的结构示意图为![]() ,可知Z为Na元素;以此分析解答。
,可知Z为Na元素;以此分析解答。
(1)由 X原子结构示意图为![]() 可知,a=7,质子数为7的元素为氮,元素符号为N;由Y元素最外层电子数是次外层电子数的2倍,所以Y元素为碳元素,其最简单氢化物为甲烷,化学式为CH4。答案:N; CH4;
可知,a=7,质子数为7的元素为氮,元素符号为N;由Y元素最外层电子数是次外层电子数的2倍,所以Y元素为碳元素,其最简单氢化物为甲烷,化学式为CH4。答案:N; CH4;
(2)由Z的原子核内含有12个中子,且其离子的结构示意图为![]() ,可知Z为Na元素,其原子的相对原子质量为23;答案:23;
,可知Z为Na元素,其原子的相对原子质量为23;答案:23;
(3)X为N元素,最高价氧化物对应的水化物为HNO3;Z为Na元素,最高价氧化物对应的水化物为NaOH,两者相互反应的离子方程式为H++OH-=H2O。答案:H++OH-=H2O;
(4) 由Y元素为碳,最高价氧化物为CO2;Z元素为Na,最高价氧化物为Na2O和Na2O2,两者发生氧化还原反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2,答案:2CO2+2Na2O2=2Na2CO3+O2。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验主要仪器和试剂的选择不能达到实验目的的是
选项 | 主要仪器 | 试剂 | 实验目的 |
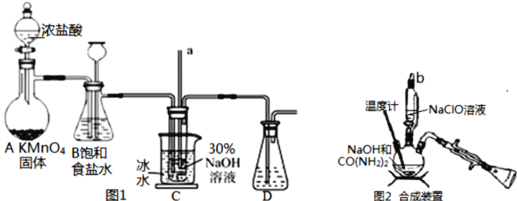
A | 烧瓶、长颈漏斗、酒精灯、导管 | 软锰矿与浓盐酸 | 制取并收集干燥的氯气 |
B | 酒精灯、玻璃棒、蒸发皿、三脚架 |
| 蒸发溶液得到晶体 |
C | 圆底烧瓶、导气管、烧杯、铁架台 | 干燥的氨气、水 | 模拟喷泉实验 |
D | 铁丝、蓝色钴玻璃、酒精灯 | 盐酸、待测液 | 焰色反应实验 |
A.AB.BC.CD.D