题目内容
【题目】工业上用铝土矿(主要成分是Al2O3、Fe2O3、SiO2)提纯Al2O3做冶炼铝的原料,提取的操作过程可用以下流程图表示:
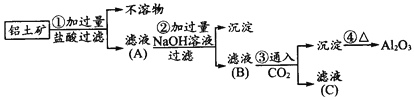
(1)请写出下列反应的化学方程式:②_________________、 _________________。③____________。
(2)若①步没有过滤操作而直接进入步骤②,对后面的操作会有什么影响?________________________。
【答案】FeCl3+3NaOH=Fe(OH)3↓+3NaCl AlCl3+4NaOH=3NaCl+NaAlO2+2H2O 2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓或NaAlO2+CO2+2H2O=NaHCO3+Al(OH)3↓ ①中的不溶物SiO2在操作②中会被NaOH溶解,造成所得Al2O3中混有SiO2
【解析】
铝土矿(主要成分是Al2O3、Fe2O3、SiO2)中加入过量的盐酸,Al2O3、Fe2O3被溶解生成氯化铁和氯化铝,二氧化硅不溶;滤液中加入过量的氢氧化钠,得到偏铝酸钠溶液和氢氧化铁沉淀;偏铝酸钠溶液中通入二氧化碳生成氢氧化铝沉淀,滤液中含有碳酸钠或碳酸氢钠。据此分析解答。
(1)根据上述分析,步骤②中氯化铝和氯化铜与过量的氢氧化钠反应生成偏铝酸钠和氢氧化铁沉淀,反应的方程式有:FeCl3+3NaOH=Fe(OH)3↓+3NaCl、AlCl3+4NaOH=3NaCl+NaAlO2+2H2O;步骤③中偏铝酸钠与二氧化碳反应生成氢氧化铝沉淀,反应的方程式为:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓或NaAlO2+CO2+2H2O=NaHCO3+Al(OH)3↓,故答案为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;AlCl3+4NaOH=3NaCl+NaAlO2+2H2O;2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓或NaAlO2+CO2+2H2O=NaHCO3+Al(OH)3↓;
(2)步骤①不溶物SiO2在步骤②中被NaOH溶解,最后得到的Al2O3中含有SiO2导致氧化铝不纯,故答案为:步骤①不溶物SiO2在步骤②中被NaOH溶解,最后得到的Al2O3中混有SiO2。

【题目】在2 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为______________(填“吸热”或“放热”)反应。
(2)能判断该反应是否达到化学平衡状态的依据是________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。该温度下,若向该容器中充入n(CO2)=1 mol,n(H2)=1 mol,4 min末达到平衡,CO2的转化率为_____________,H2的体积分数为_________。
【题目】根据题意完成下列问题:
(1)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g) ![]() CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
已知:2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:_______________________________________。
(2)随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NO x、SO2、CO等大气污染气体的处理具有重要意义。用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)![]() N2(g)+CO2(g)。某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①则从反应开始到20mi时,以NO表示的平均反应速率= ________,该温度下该反应的平衡常数K=____(保留两位小数)
②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是_____(写一条即可)。
③下列描述中能说明上述反应已达平衡的是__________;
A、容器内气体的平均摩尔质量保持不变
B、2v(NO)正=v(N2)逆
C、容器中气体的压强保持不变
D、单位时间内生成nmolCO2的同时生成2nmolNO
(3)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42-, 而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ =4Fe3+ + 2H2O,则另一反应的离子方程式为_______________
(4)有学者想以如图所示装置用原电池原理将SO2转化为重要的化工原料。

若A为SO2,B为O2,C为H2SO4,则负极反应式为_______________________________,电池总反应式为________________________。