题目内容
11.W、X、Y、Z为原子序数依次增大的同周期的短周期元素.已知W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水.下列判断正确的是( )| A. | W、Y、Z三种元素的最高价氧化物的水化物可能有两种是强碱、一种是强酸 | |
| B. | Z元素在第3周期第ⅥA族 | |
| C. | W、Y、Z三种元素有两种是金属、一种是非金属 | |
| D. | W、X、Y三种元素最高价氧化物对应水化物的碱性依次增强 |
分析 W、X、Y、Z为同一短周期元素,原子序数依次增大,W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,应氢氧化铝与强碱、强酸的反应,则W为Na,Y为Al,X为Mg,而Z的最外层电子数为11-1-3=7,故Z为Cl,以此来解答.
解答 解:W、X、Y、Z为同一短周期元素,原子序数依次增大,W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,应氢氧化铝与强碱、强酸的反应,则W为Na,Y为Al,X为Mg,而Z的最外层电子数为11-1-3=7,故Z为Cl.
A.W、Y、Z三种元素的最高价氧化物的水化物分别为NaOH、Al(OH)3、HClO4,分别为强碱、弱碱、强酸,故A错误;
B.Z为Cl,则在第三周期ⅤⅡA族,故B错误;
C.W为Na,Y为Al,Z为Cl,前两者为金属、后一种为非金属,故C正确;
D.W、X、Y三种元素最高价氧化物对应水化物分别为氢氧化钠、氢氧化镁、氢氧化铝,碱性依次减弱,故D错误,
故选C.
点评 本题考查位置结构性质关系应用,推断元素是解答本题的关键,题目难度不大,注意根据“短周期元素及最高价氧化物的水化物之间两两皆能反应,均生成盐和水”进行推断.

练习册系列答案
相关题目
1.某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A. | 正极为Fe,负极为Zn,电解质Fe2(SO4)3溶液 | |
| B. | 正极为Cu,负极为Fe,电解质FeCl3溶液 | |
| C. | 正极为Cu,负极为Fe,电解质Fe(NO3)3溶液 | |
| D. | 正极为Ag,负极为Fe,电解质Fe2(SO4)3溶液 |
2.下列有关说法错误的是( )
| A. | 石油和天然气的主要成分都是碳氢化合物 | |
| B. | 甲烷和乙烯都能与Cl2发生反应 | |
| C. | 乙烯可以合成有机高分子材料 | |
| D. | 苯和乙醇都能被酸性KMnO4溶液氧化而使KMnO4溶液褪色 |
19.某有机物结构如图所示,关于该有机物下列说法正确的是( )
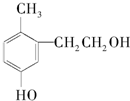

| A. | 该物质在加热条件下可以与铜反应生成一种具有醛基的化合物 | |
| B. | 1 mol该物质能与溴水反应消耗3 mol Br2发生取代反应 | |
| C. | 1 mol该有机物能与足量金属钠反应生成0.5 mol H2 | |
| D. | 1 mol该有机物能与2 mol NaOH反应 |
20.下列条件下的反应,放出氢气最快的是( )
| 金属(相同粉末状) 和物质的量(mol) | 酸的浓度和体积(mL) | 反应温度 | |||
| A | Fe | 0.1 | 3mol/L HCl | 10 | 20℃ |
| B | Al | 0.1 | 3mol/L HCl | 10 | 20℃ |
| C | Cu | 0.1 | 4mol/L H2SO4 | 10 | 20℃ |
| D | Mg | 0.1 | 稀6mol/L HNO3 | 10 | 20℃ |
| A. | A | B. | B | C. | C | D. | D |
1.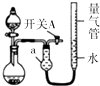 某同学设计图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
某同学设计图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
(1)仪器a的名称是干燥管.
(2)检查该装置的气密性的方法是:关闭开关A和分液漏斗活塞,微热烧瓶,量气管右端液面升高,说明气密性良好.
(3)该同学认为实验①可通过收集测量NO2气体的体积,来探究Cu样品的纯度.请问是否可行否(填“是”或“否”);实验①中烧瓶内反应的离子方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(4)实验②中,量气管中的液体最好是D:
A.H2O B.饱和NaHCO3溶液C.饱和Na2CO3溶液 D.CCl4
(5)本实验应对量气管多次读数,读数时应注意:
①恢复至室温,②保持量气管内液体与干燥管内液体液面相平,③视线与凹液面最低处相平.
(6)实验③获得以下数据(所有气体体积均已换算成标准状况).
根据上述合理数据计算粗Mg中Mg的质量分数72%.
 某同学设计图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
某同学设计图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| ① | Cu、浓HNO3 | H2O | |
| ② | CaO固体、浓氨水 | NH3 | |
| ③ | 粗镁、稀H2SO4 (足量)[杂质不与硫酸反应] | H2 | H2O |
(2)检查该装置的气密性的方法是:关闭开关A和分液漏斗活塞,微热烧瓶,量气管右端液面升高,说明气密性良好.
(3)该同学认为实验①可通过收集测量NO2气体的体积,来探究Cu样品的纯度.请问是否可行否(填“是”或“否”);实验①中烧瓶内反应的离子方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(4)实验②中,量气管中的液体最好是D:
A.H2O B.饱和NaHCO3溶液C.饱和Na2CO3溶液 D.CCl4
(5)本实验应对量气管多次读数,读数时应注意:
①恢复至室温,②保持量气管内液体与干燥管内液体液面相平,③视线与凹液面最低处相平.
(6)实验③获得以下数据(所有气体体积均已换算成标准状况).
| 编号 | 镁(含杂质)质量 | 量气管第一次读数 | 量气管第二次读数 |
| 1 | 0.5g | 10.0mL | 346.5mL |
| 2 | 0.5g | 10.0mL | 335.0mL |
| 3 | 0.5g | 10.0mL | 345.5mL |
 .
.