题目内容
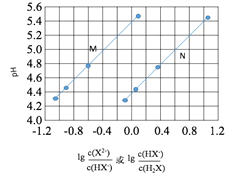
【题目】磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-、和PO43-四种粒子形式存在,当溶液的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化。下图是H3PO4溶液中,各种粒子的物质的量分数δ随pH的变化曲线:
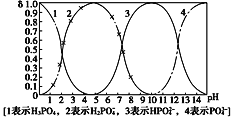
(1)向Na3PO4溶液中逐滴滴入稀盐酸,当pH从9降到6的过程中发生的主要反应的离子方程式为________。当pH=7时,溶液中主要存在的阴离子(OH-离子除外)是__________。
(2)从图中推断NaH2PO4溶液呈______性(填“酸”“碱”或“中”),其原因是_________。
(3)在Na3PO4溶液中,c(Na+)/c(PO43-)______3(填“>”“=”或“<”);向该溶液中滴入几滴浓KOH溶液后,c(Na+)/c(PO43-)的值减小,原因是____。
【答案】HPO42-+H+=H2PO4- H2PO4-和HPO42- 酸 H2PO4-在溶液中的电离程度大于水解程度 > KOH抑制了PO43-的水解
【解析】
(1)根据P原子守恒分析;(2)当向溶液中滴加稀盐酸时, 根据溶液中离子的变化判断发生的离子反应;当pH=7时,根据图象确定溶液中存在的阴离子;(3)根据图象分析,当溶液中存在H2PO4-时溶液的pH值确定溶液的酸碱性,从而确定H2PO4-的电离程度和水解程度的相对大小;(4)先根据磷酸钠盐的类型确定钠离子和磷酸根离子的关系,再根据外界条件对水解平衡的影响分析。
(1)根据图象知,当向溶液中滴加稀盐酸时,溶液中H2PO4-增加,HPO42-减少,所以是溶液中的HPO42-和氢离子发生反应生成H2PO4-,离子方程式为:HPO42-+H+=H2PO4-;当pH=7时,根据图象知,溶液中存在的阴离子为H2PO4-、HPO42-;
(2)根据图象知,当溶液中存在H2PO4-时,溶液呈酸性,说明H2PO4-在溶液中的电离程度大于水解程度,导致溶液中氢离子浓度大于氢氧根离子的浓度,答案:酸;H2PO4-在溶液中的电离程度大于水解程度。
(3)磷酸钠是强碱弱酸盐,所以弱酸根离子能发生水解,导致溶液中c(Na+)/c(PO43-)>3;PO43-+H2O![]() HPO2-+OH-,当向溶液中滴入几滴浓KOH溶液后,根据勒夏特列原理知,水解平衡向逆反应方向移动,所以导致溶液中磷酸根离子的浓度增大,故c(Na+)/c(PO43-)的值减小。
HPO2-+OH-,当向溶液中滴入几滴浓KOH溶液后,根据勒夏特列原理知,水解平衡向逆反应方向移动,所以导致溶液中磷酸根离子的浓度增大,故c(Na+)/c(PO43-)的值减小。