题目内容
2.已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O(1)标出上述反应电子转移的方向和数目
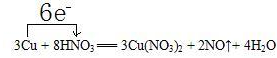 .
.(2)上述反应中氧化产物是Cu(NO3)2,上述反应中氧化剂与还原剂的物质的量之比为2:3.
(3)若反应中转移了0.6mol电子,产生的气体在标准状况下的体积是44.8L.
分析 (1)化合价升高元素失电子,化合价降低元素得到电子,化合价升高数=化合价降低数=转移电子数;
(2)根据离子方程式的书写方法来书写离子方程式,在氧化还原反应中,化合价降低元素所在的反应物是氧化剂,对应产物是还原产物,化合价升高元素所在的反应物是还原剂,对应产物是氧化产物,根据硝酸的作用以及方程式进行计算;
(3)根据反应转移电子的数目以及产生NO关系来计算即可.
解答 解:(1)化合价升高元素Cu失电子,化合价降低元素N得到电子,化合价升高数=化合价降低数=转移电子数=6,电子转移情况如下: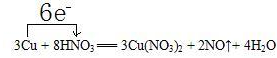 ,故答案为:
,故答案为: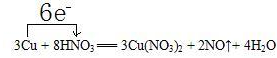 ;
;
(2)铜和硝酸反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,化合价降低元素的N元素所在的反应物HNO3是氧化剂,对应的产物NO是还原产物,化合价升高元素的Cu元素所在的反应物Cu是还原剂,Cu(NO3)2是氧化产物,氧化剂与还原剂的物质的量之比为2:3,故答案为:Cu(NO3)2;2:3;
(3)在参加反应的8mol硝酸中,被还原的硝酸的物质的量为2mol,生成NO的物质的量是2mol,转移电子是6mol,若反应中转移了0.6mol电子,产生的气体的物质的量是0.2mol,在标准状况下的体积是0.2mol×22.4L/mol=44.8L.
故答案为:44.8L.
点评 本题考查学生氧化还原反应的有关知识,注意基本概念和电子转移知识的掌握是关键,难度不大.

练习册系列答案
相关题目
12.向H2SO4、CuCl2混合溶液中投入足量的铁粉,经充分反应后,过滤、洗涤、干燥、称重,知所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比( )
| A. | 1:2 | B. | 1:7 | C. | 7:1 | D. | 1:14 |
13.在Fe、Fe2+、Fe3+三种粒子中,具有相同的( )
| A. | 电荷数 | B. | 最外层电子数 | C. | 核电荷数 | D. | 核外电子数 |
7.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氢氧化钡溶液滴入稀硫酸中:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 二氧化硫与足量氢氧化钠溶液反应 SO2+2OHˉ=SO32-+H2O | |
| D. | 铝与氢氧化钠溶液反应:Al+2OH-═2A1O${\;}_{2}^{-}$+H2↑ |
11.配制250mL 0、1000mol/LNaCl溶液时,下列操作会使配得溶液中NaCl的物质的量浓度偏大的是( )
| A. | 移液后未洗涤烧杯 | |
| B. | 在容量瓶中进行定容时,仰视刻度线 | |
| C. | 在容量瓶中进行定容时,俯视刻度线 | |
| D. | 定容后摇匀,发现液面低于刻度线,再加水至刻度线 |

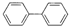 分子式:C12H10
分子式:C12H10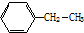 其苯环上的一氯代物有_5种
其苯环上的一氯代物有_5种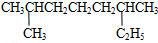 的系统命名是2,6-二甲基辛烷
的系统命名是2,6-二甲基辛烷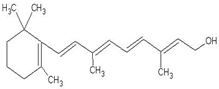 1mol该物质消耗5molH2,5molBr21molNa
1mol该物质消耗5molH2,5molBr21molNa 制备水杨酸对正辛基苯基酯(
制备水杨酸对正辛基苯基酯(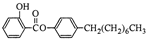 )如下:
)如下: (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑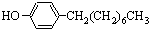 ],温度控制在100℃左右,不断搅拌.
],温度控制在100℃左右,不断搅拌. .
.