题目内容
9. (1)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,是放热反应,当1mol Cl2参与反应时释放145kJ的热量,写出这个反应的热化学方程式:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•mol-1.
(1)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,是放热反应,当1mol Cl2参与反应时释放145kJ的热量,写出这个反应的热化学方程式:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•mol-1.(2)Ag2O2是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag.
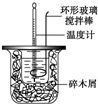
(3)50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
若某同学利用上述装置做实验,有些操作不规范,造成测得的结果偏低,请你分析结果偏低的原因可能是ABDF(填字母代号).
A.测量盐酸和NaOH溶液反应后的温度时,温度计温度达到最高值
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天,室温较高
D.将50mL 0.55mol•L-1的氢氧化钠溶液换成了50mL 0.55mol•L-1的氨水
E.在量取盐酸时仰视读数
F.大烧杯的盖板中间小孔太大
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化成液态水放热2.444kJ,氢气的燃烧热为285.8kJ•mol-1.
分析 (1)反应热与反应计量数呈正比,依据热化学方程式书写方法写出,标注物质聚集状态和对应焓变;
(2)电池放电时正极的Ag2O2 转化为Ag,负极的Zn转化为K2Zn(OH)4,反应还应有KOH参加,依据转化写出电池反应;
(3)A.测量盐酸和NaOH溶液反应后的温度时,温度计温度达到最高值,最高温度可能偏小;
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会造成热量散失;
C.做本实验的当天,室温较高,与测定温度无关;
D.氨水是弱电解质,电离要吸热;
E.在量取盐酸时仰视读数,盐酸的体积偏大,放出的热量偏多;
F.大烧杯的盖板中间小孔太大,会造成热量散失;
(4)氢气的燃烧热是值1mol氢气完全燃烧生成液态水放出的热量;根据m=nM计算1mol水的质量为18g,进而计算1mol气态水转化成液态水放出的热量,结合氢气与氧气反应生成气态水的反应热计算生成液态水的反应热.
解答 解:(1)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1molCl2参与反应时释放145kJ的热量,2mol氯气完全反应放热290 kJ,热化学方程式为:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290 kJ•mol-1;
故答案为:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290 kJ•mol-1;
(2)电池放电时正极的Ag2O2 转化为Ag,负极的Zn转化为K2Zn(OH)4,正极电极反应式为Ag2O2+4e-+2H2O═2Ag+4OH-,负极电极反应式为2Zn-4e-+8OH-═2Zn(OH)42-,反应还应有KOH参加,反应的总方程式为:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag;
故答案为:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag;
(3)A.测量盐酸和NaOH溶液反应后的温度时,温度计温度达到最高值,最高温度可能偏小,温度差偏小,中和热的数值偏小,故A正确;
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会造成热量散失,中和热的数值偏小,故B正确;
C.做本实验的当天,室温较高,与测定温度无关,不影响中和热的数值,故C错误;
D.氨水是弱电解质,电离要吸热,测得的热量偏小,中和热的数值偏小,故D正确;
E.在量取盐酸时仰视读数,盐酸的体积偏大,放出的热量偏多,中和热的数值偏大,故E错误;
F.大烧杯的盖板中间小孔太大,会造成热量散失,中和热的数值偏小,故F正确;
故答案为:ABDF;
(4)氢气和氧气反应生成1mol水蒸气放热241.8kJ,该反应的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8kJ/mol;
1g水蒸气转化成液态水放热2.44kJ,故18g水蒸气转化成液态水放出热量2.444kJ×18=43.992kJ,故反应H2(g)+$\frac{1}{2}$O2(g)═H2O(l)的反应热△H=-(241.8kJ/mol+43.992kJ/mol)=-285.8kJ/mol,故氢气的燃烧热为285.8kJ/mol;
故答案为:285.8.
点评 本题考查热化学方程式的书写,中和热的测定原理,反应热的计算,难度不大,注意掌握热化学方程式的书写,物质聚集状态的分析判断,盖斯定律的计算应用,题目较简单.

 小学课时特训系列答案
小学课时特训系列答案| A. | 在常温常压下,11.2 L 氯化氢气体含有的分子数为0.5 NA | |
| B. | 1.7g 氨气(NH3)所含原子数目为 0.4NA | |
| C. | 同温同压时,相同体积的任何气体单质所含的原子数相同 | |
| D. | 1 L 1 mol•L-1的Na2SO4溶液中含粒子的总数为3NA |
| A. | 充电时铁做负极,NiO2做正极 | |
| B. | 放电时阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH- | |
| C. | 放电时,电解质溶液中的阴离子是向正极方向移动 | |
| D. | 蓄电池的两个电极必须浸入在碱性溶液中 |
| 元素代号 | X | Y | Z | Q | R |
| 原子半径/10-10m | 0.37 | 0.66 | 0.70 | 0.88 | 0.99 |
| 主要化合价 | +1 | -2 | +5、-3 | +3 | +7、-1 |
| A. | 元素X、Y、Z形成的化合物一定是离子化合物 | |
| B. | X元素和R元素形成的化合物XR是18电子的分子 | |
| C. | 化合物QR3分子中各原子均满足8电子稳定结构 | |
| D. | 元素Z的氧化物对应水化物一定为强酸 |
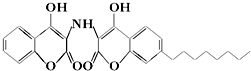
| A. | 分子式为C26H28O6N | |
| B. | 遇FeCl3溶液不能发生显色反应 | |
| C. | 1mol该物质最多能与8mol氢气发生加成反应 | |
| D. | 1mol该物质最多能与4molNaOH溶液完全反应 |
| A. | 若甲为强酸、乙为弱酸,则c(甲):c(乙)=10:1 | |
| B. | 若甲为弱酸,乙为强酸,则一定满足c(甲)>c(乙) | |
| C. | 若甲为强酸,乙为弱酸,则其物质的量浓度不可能相等 | |
| D. | 若甲、乙均为弱酸,则甲酸的电离常数一定比乙酸大 |
