题目内容
【题目】(写出计算步骤)已知可逆反应:M(g)+N(g)![]() P(g)+Q(g),△H>0请回答下列问题:
P(g)+Q(g),△H>0请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol·L-1,c(N)=2.4mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为多少______?平衡常数?__
(2)若反应温度不变,反应物的起始浓度分别为:c(M)=4mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2mol·L-1,a=?;________
(3)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=bmolL-1,,达到平衡后,M的转化率为多少?________
【答案】25%; 0.5 6 41%
【解析】
由题意建立三段式求解可得。
(1)由题意建立如下三段式:

则N的转化率为![]() ×100%=25%,化学平衡常数K=
×100%=25%,化学平衡常数K=![]() =0.5,故答案为:25%;0.5;
=0.5,故答案为:25%;0.5;
(2)由题意建立如下三段式:
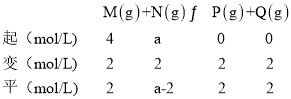
温度不变,化学平衡常数不变,则![]() =0.5,解得a=6mol·L-1,故答案为:6;
=0.5,解得a=6mol·L-1,故答案为:6;
(3)设M的转化率为x,由题意建立如下三段式:

温度不变,化学平衡常数不变,则![]() =0.5,解得x=0.41b,则M的转化率为41%,故答案为:41%。
=0.5,解得x=0.41b,则M的转化率为41%,故答案为:41%。
![]()

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目