题目内容
【题目】氯气是重要的化工原料。
(1)工业上常用_______法生产氯气,写出发生反应的化学方程式:_________________________。
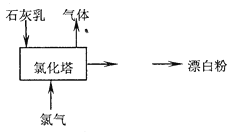
(2)工业上常用石灰乳和氯气反应制取漂白粉,化学反应方程式是____________________。部分流程如右图所示,其主要设备是氯化塔,,塔从上到下分四层.将含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入,这样加科的目的是___________________________________。
(3)某科研小组在实验室用较浓的KOH溶液直接吸收氯气,研究发现反应进行一段时间后开始出现KClO3并逐渐增多,产生KClO3的离子方程式是___________________,其原因可能是_____________________,由此可知(2)中氯化塔设计为四层是为了减少生产中类似副反应的发生。
【答案】(1)电解饱和食盐水2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O 增大反应物间的接触面积,使反应充分进行(3)6OH-+3Cl2=5Cl-+ClO3-+3H2O;反应放热使温度升高所致
【解析】
试题分析:(1)工业用电解饱和食盐水的方法制备氯气,电解饱和食盐水反应生成NaOH、H2、Cl2,该反应为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;(2)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入时接触面积增大,使反应充分进行;(3)较浓的KOH溶液直接吸收氯气,生成KCl、KClO3、水,离子反应为6OH-+3Cl2=5Cl-+ClO3-+3H2O,发生该反应是因反应放热使温度升高所致。
2NaOH+H2↑+Cl2↑;(2)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,含有3%~6%水分的熟石灰从塔顶喷洒而入,氯气从塔的最底层通入时接触面积增大,使反应充分进行;(3)较浓的KOH溶液直接吸收氯气,生成KCl、KClO3、水,离子反应为6OH-+3Cl2=5Cl-+ClO3-+3H2O,发生该反应是因反应放热使温度升高所致。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
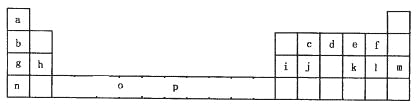
试回答下列问题:
(1)元素p为26号元素,请画出其基态原子外围电子排布图______________;
(2)e与a反应的产物的分子中中心原子的杂化形式为________________;该分子是_________(填“极性”或“非极性”)分子。
(3)上表中元素基态原子的第一电离最大的元素是__________。(用元素符号表示)
(4)o、p两元素的部分电离能数据列于下表:
元 素 | O | P | |
电离能 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难,对此,你的解释是______________;