题目内容
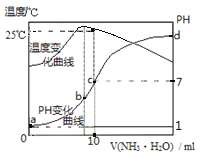
【题目】在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是
A.a点KW=1.0×10-14
B.水的电离程度:b>c>a>d
C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.25℃时,一水合氨的电离平衡常数为10-7/(10n-1)(用n表示)
【答案】D
【解析】
A、水的离子积与温度有关,a点时溶液温度小于25度,则水的离子积KW小于1.0×10-14,错误,不选A;
B、b点溶液温度最高,说明此时两溶液恰好反应生成氯化铵,铵根离子水解促进水的电离,则ad两点后抑制了水的电离,则b点水的电离程度最大,由于d点混合溶液的pH未知,则无法判断ad两点的水的电离程度,错误,不选B;
C、b点时溶液显酸性,则氢离子浓度大于氢氧根离子浓度,根据电荷守恒可知,氯离子浓度大于铵根离子浓度,溶液中的离子浓度顺序为:c(Cl-)>c(NH4+)> c(H+)>c(OH-),所以错误,不选C;
D、根据图像可知,25度时溶液的pH=7,则c(H+)=c(OH-)=10-7mol/L,铵根离子浓度为0.05mol/L,一水合氨的浓度为0.5n-0.05mol/L,则一水合氨的电离平衡常数= c(NH4+) c(OH-)/ c(NH3·H2O)= 0.05×10-7/(0.5n-0.05)=10-7/(10n-1)正确;
答案选D。

【题目】某同学用标准NaOH溶液来测定未知浓度的盐酸的浓度:
(1)先配制250mL 0.5mol/L的NaOH标准溶液所需的称量的质量NaOH为________ g,
需要的主要玻璃仪器有玻璃棒、量烧杯、胶头滴管、量筒和___________。
(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用NaOH溶液滴定到终点。在锥形瓶的待测液中滴加2~3滴酚酞试液,并开始滴定。
手眼:左手控制滴定管活塞,右手摇动锥形瓶,眼睛____________;
滴速:先快后慢,当接近终点时,应一滴一摇。滴定终点的判断:___________,即到终点,读出体积并记录数据。
(3)该同学进行了三次实验,实验数据如下表:
实验编号 | 盐酸的体积(mL) | 标准NaOH溶液的体积(mL) |
① | 均是20.00 | 16.90 |
② | 17.10 | |
③ | 18.20 |
滴定中误差较大的是第______次实验。造成这种误差的可能原因是__________(填选项编号)
a.滴定管在盛装标准NaOH溶液前未润洗
b.在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
c.达到滴定终点时,俯视溶液凹液面最低点读数
d.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f.滴定开始前盛装标准NaOH溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
(4)该同学所测得盐酸的物质的量浓度为_________。(结果保留三位小数)。