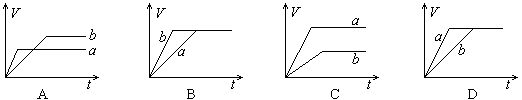题目内容
下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 |
| B.双氧水制氧气时加入少量二氧化锰 |
| C.试管中进行镁和水反应时,稍微加热 |
| D.铁粉代替铁钉与稀硫酸反应制取氢气 |
A
解析试题分析:影响化学反应速率的因素:内因:物质本身的性质,这个是起到决定性的作用。外因:温度、浓度、压强、催化剂、反应物的接触面积。升高温度反应速率加快,降低温度反应速率减慢。增大反应物的浓度,反应速率加快,压强一般是对于有其他参与的反应才有影响,增大压强反应速率加快。催化剂一般情况下如果没有特别说明,则认为是加快反应速率。增大反应物接触面积,一般的做法是把反应物进行碾碎成粉末。则它的反应速率也会加快。故A选项降低温度反应速率减慢。B选项加催化剂加快反应速率C选项增大温度,反应速率加快D选项增大反应物的接触面积反应速率加快
考点:影响化学反应速率的相关因素

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列过程中,需要增大化学反应速率的是( )
| A.钢铁腐蚀 | B.食物腐败 | C.塑料老化 | D.工业合成氨 |
已知反应3A(g)+B(g)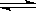 C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )
C(s)+4D(g) ΔH<0,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是( )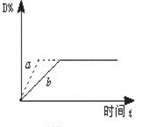
①增大B的浓度 ②升高反应温度
③缩小反应容器的体积(加压) ④加入催化剂
| A.①② | B.①③ | C.②③ | D.③④ |
一定温度下,在体积一定的密闭容器中进行的可逆反应:C(s) + CO2(g)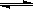 2CO(g),不能判断反应已经达到化学平衡状态的是
2CO(g),不能判断反应已经达到化学平衡状态的是
| A.v(CO2)= v(CO) | B.容器中总压强不变 |
| C.容器中混合气体的密度不变 | D.容器中CO的体积分数不变 |
把下列4种Na2S2O3溶液和相应体积的水,分别加入4个盛有20 mL 2 mol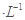 硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应:
硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应: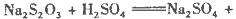
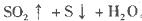 其中最早出现明显浑浊的是
其中最早出现明显浑浊的是
A.25 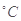 .20 mL 3 mol .20 mL 3 mol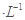 的Na2S2O3溶液,25 mL蒸馏水 的Na2S2O3溶液,25 mL蒸馏水 |
B.0 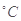 .30 mL 2 mol .30 mL 2 mol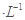 的Na2S2O3溶液,15 mL蒸馏水 的Na2S2O3溶液,15 mL蒸馏水 |
C.25 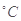 .10 mL 4 mol .10 mL 4 mol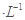 的Na2S2O3溶液,35 mL蒸馏水 的Na2S2O3溶液,35 mL蒸馏水 |
D.0 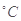 .10 mL 2mol .10 mL 2mol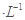 的Na2S2O3溶液,35 mL蒸馏水 的Na2S2O3溶液,35 mL蒸馏水 |
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的是( )
R(g)+S(g)在恒温下已达到平衡的是( )
| A.反应容器内的压强不随时间改变 | B.反应容器内P、Q、R、S四者共存 |
| C.P的生成速率和S的生成速率相等 | D.反应容器内的气体总物质的量不随时间变化 |