题目内容
7.下列事实不能说明非金属性Cl>I的是( )| A. | Cl2+2I-→2Cl-+I2 | B. | 酸性:HClO3>HIO3 | C. | 酸性:HClO4>HIO4 | D. | 稳定性:HCl>HI |
分析 元素非金属性越强,其单质得电子能力越强、其氢化物的稳定性越强、其最高价氧化物的水化物酸性越强,据此分析解答.
解答 解:A.元素的非金属性越强,其单质的氧化性氧气,该反应中氧化性Cl2>I2,所以能说明非金属性Cl>I,故A不选;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,HClO3、HIO3不是Cl、I的最高价氧化物的水化物,所以不能据此判断非金属性强弱,故B选;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,HClO4、HIO4是Cl、I的最高价氧化物的水化物,所以能据此判断非金属性强弱,故C不选;
D.元素非金属性越强,其氢化物的稳定性越强,稳定性HCl>HI,则非金属性Cl>I,所以能据此判断非金属性强弱,故D不选;
故选B.
点评 本题考查非金属性强弱判断,为高频考点,明确非金属性强弱与单质氧化性、氢化物的稳定性、最高价含氧酸酸性之间关系是解本题关键,注意:不能根据一般的含氧酸判断非金属性强弱,为易错点.

练习册系列答案
相关题目
17.下列行为符合安全要求的是( )
| A. | 配制稀硫酸时将水倒入浓硫酸中并不断搅拌 | |
| B. | 不慎洒出的酒精在桌上着火时,立即用水扑灭 | |
| C. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 | |
| D. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 |
18.下列关于钠的叙述中,正确的是( )
| A. | 常温下,钠露置在空气中易被氧气氧化为过氧化钠,因此应保存在煤油里 | |
| B. | 钠是强还原剂,它能从盐溶液中置换出金属活动顺序表中排在钠后面的金属 | |
| C. | 钠蒸气充入灯泡中制成钠灯,常用于公路照明 | |
| D. | 金属钠着火时,能用水来灭火 |
15.称取两份铝粉,第一份加入足量的浓NaOH(aq),第二份加入足量的HCl(aq),如果放出等体积的气体(在同温同压下测定),则两份铝粉的质量之比为( )
| A. | 1:2 | B. | 1:3 | C. | 3:2 | D. | 1:1 |
2.Fe3+、SO42-、Al3+和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,X可能是( )
| A. | Br- | B. | OH- | C. | HCO3- | D. | NH4+ |
8.X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A. | 原子半径:Y>Z>W | |
| B. | ZW2电子式为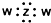 | |
| C. | 片状Y在空气中点燃时现象不剧烈 | |
| D. | 已知XW2熔点为-107℃、沸点为12.5℃,熔融时不导电,可说明固态XW2为共价化合物 |