题目内容
20.下列各组离子在特定条件下能够大量共存的是( )| A. | 在使石蕊试液变红的溶液中:Na+、NH4+、NO3-、AlO2- | |
| B. | 在含有较多Al3+的溶液中:Na+、K+、SO42-、HCO3- | |
| C. | 室温下,在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液中:K+、I-、Cl-、HS- | |
| D. | 在无色溶液中:SO42-、Cl-、NH4+、Na+ |
分析 A.使石蕊试液变红色的溶液呈酸性,和H+反应的离子不能大量共存;
B.在含有较多Al3+的溶液中不能大量存在和Al3+反应的离子;
C.室温下,在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液呈碱性,和OH-反应的离子不能大量共存;
D.无色溶液不含有色离子.
解答 解:A.使石蕊试液变红色的溶液呈酸性,AlO2-和H+反应而不能大量共存,故A错误;
B.在含有较多Al3+的溶液中,HCO3-和Al3+发生双水解反应而不能大量共存,故B错误;
C.室温下,在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液呈碱性,HS-和OH-反应而不能大量共存,故C错误;
D.无色溶液不含有色离子,这几种离子之间不反应且无色,所以能大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,侧重考查双水解反应、复分解反应,明确离子性质及离子共存条件是解本题关键,易错选项是B.

练习册系列答案
相关题目
10. 若将反应:Zn+H2SO4=ZnSO4+H2↑设计成原电池(如图),则下列说法不正确的是( )
若将反应:Zn+H2SO4=ZnSO4+H2↑设计成原电池(如图),则下列说法不正确的是( )
 若将反应:Zn+H2SO4=ZnSO4+H2↑设计成原电池(如图),则下列说法不正确的是( )
若将反应:Zn+H2SO4=ZnSO4+H2↑设计成原电池(如图),则下列说法不正确的是( )| A. | 该装置实现了化学能转化为电能 | B. | b 极表面发生了还原反应 | ||
| C. | c 溶液可以是ZnSO4 溶液 | D. | 盐桥中的Cl-移向右边烧杯 |
11.下列说法不正确的是( )
| A. | 发展核电、煤中加入生石灰、利用二氧化碳制造全降解塑料都能有效减少环境污染 | |
| B. | 物质变化中炭化、钝化、皂化、酯化、熔化都属于化学变化 | |
| C. | 氢键、分子间作用力、离子键和共价键均为微粒间的相互作用力 | |
| D. | 农业废弃物、城市工业有机废弃物及动物粪便中都蕴藏着丰富的生物质能 |
15.在一定条件下,将NO2和O2的混合气体12mL通入足量水中,充分反应后剩余2mL气体(同温同压下),则原混合气体中氧气的体积为( )
①1.2mL ②2.4mL ③3mL ④4mL.
①1.2mL ②2.4mL ③3mL ④4mL.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
12.要使10mL0.05mol•L-1H2SO4溶液的pH增大2,下列方法不可行的是( )
| A. | 向溶液中加入适量氯化铵固体 | |
| B. | 向溶液中加入一定体积的pH=4的盐酸 | |
| C. | 向溶液中加水至溶液体积为1000mL | |
| D. | 向溶液中加入适量醋酸钠固体 |

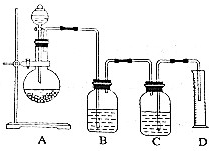 实验室可利用该装置来制取氯气,发生反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O.
实验室可利用该装置来制取氯气,发生反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O.
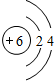 ;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式
;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式 ,用电子式表示⑤和⑧形成化合物的过程
,用电子式表示⑤和⑧形成化合物的过程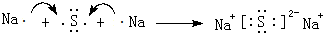 .
.