题目内容
18.由铜片、锌片和稀硫酸组成的原电池工作时,下列叙述正确的是( )| A. | 铜片电极反应:2H++2e-=H2↑ | B. | 锌片电极反应:Zn-e-=Zn2+ | ||
| C. | 铜为负极,发生还原反应 | D. | 锌为负极,发生还原反应 |
分析 在用锌片、铜片和稀硫酸组成的原电池装置中,锌片的活泼性大于铜片的活泼性,所以锌片作负极,负极上锌失电子发生氧化反应,铜片作正极,正极上氢离子得电子发生还原反应,以此解答该题.
解答 解:A.铜片作正极,正极上氢离子得电子发生还原反应,反应为2H++2e-=H2↑,故A正确;
B.锌片作负极,负极上锌失电子发生氧化反应,反应为Zn-2e-=Zn2+,故B错误;
C.铜片作正极,正极上氢离子得电子发生还原反应,故C错误;
D.锌片作负极,负极上锌失电子发生氧化反应,故D错误.
故选A.
点评 本题考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池的组成条件和工作原理,把握电极的判断和电极方程式的书写,难度不大.

练习册系列答案
相关题目
8.食盐中的加碘剂选用的是碘酸钾(KIO3)而不是碘化钾(KI).实验室可用采用如图1实验流程制备碘酸钾.
(1)操作①和操作③的名称分别为过滤、蒸馏.操作②所用到的玻璃仪器有分液漏斗.
(2)由单质碘制备碘酸钾的离子方程式为I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O.
(3)问题讨论:在选择试剂X时,甲同学只选择了H2O2,乙同学除了选择H2O2外还加入了少量H2SO4,并做如下实验:
①根据乙同学选择的试剂X,写出M→N离子方程式2I-+H2O2+2H+=I2+2H2O;
②由甲、乙两同学的实验结果,你能得到的结论是:溶液的酸碱性会影响H2O2的氧化能力.
(4)实验探究:受(3)实验的启发,甲、乙同学继续探究KI固体在空气中放置变质的原因.
甲同学认为:KI变质只与空气中的O2和H2O有关;
乙同学认为:KI变质除了与O2和H2O有关外,还应与空气中的某种气体成分Y有关.
甲、乙同学分别用如图2所示装置进行实验,一段时间后取出燃烧匙中的固体,在试管中溶于淀粉溶液,结构发现甲同学试管中溶液未变蓝,而乙同学试管中溶液明显变蓝.
①气体Y为CO2(填化学式).
②KI固体在空气中变质的化学方程式为4KI+O2+2CO2=2K2CO3+I2.

(1)操作①和操作③的名称分别为过滤、蒸馏.操作②所用到的玻璃仪器有分液漏斗.
(2)由单质碘制备碘酸钾的离子方程式为I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O.
(3)问题讨论:在选择试剂X时,甲同学只选择了H2O2,乙同学除了选择H2O2外还加入了少量H2SO4,并做如下实验:
| 甲 | 乙 | |
| 所选试剂X | H2O2 | H2O2,少量稀H2SO4 |
| 操作 | 向5mLM和淀粉的混合溶液中加入1mL H2O2 | 向5mLM和淀粉的混合溶液中加入1mL H2O2,再加少量稀H2SO4 |
| 实验现象 | 几秒钟后,溶液呈现很淡的蓝色 | 溶液立刻呈现较深的蓝色 |
②由甲、乙两同学的实验结果,你能得到的结论是:溶液的酸碱性会影响H2O2的氧化能力.
(4)实验探究:受(3)实验的启发,甲、乙同学继续探究KI固体在空气中放置变质的原因.
甲同学认为:KI变质只与空气中的O2和H2O有关;
乙同学认为:KI变质除了与O2和H2O有关外,还应与空气中的某种气体成分Y有关.
甲、乙同学分别用如图2所示装置进行实验,一段时间后取出燃烧匙中的固体,在试管中溶于淀粉溶液,结构发现甲同学试管中溶液未变蓝,而乙同学试管中溶液明显变蓝.
①气体Y为CO2(填化学式).
②KI固体在空气中变质的化学方程式为4KI+O2+2CO2=2K2CO3+I2.
9.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见右表.回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内.
(2)反应Ⅱ中加入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.
(3)实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2体积为 11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(4)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
(6)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol•L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.已知:3Fe3++2I-═2Fe2++I2 I2+2S2O32-═2I-+S4O62-.则溶液中铁元素的总含量为5.6g•L-1.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会偏高 (填“偏高”“偏低”“不变”).

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见右表.回答下列问题:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(2)反应Ⅱ中加入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.
(3)实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2体积为 11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(4)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
(6)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000mol•L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.已知:3Fe3++2I-═2Fe2++I2 I2+2S2O32-═2I-+S4O62-.则溶液中铁元素的总含量为5.6g•L-1.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会偏高 (填“偏高”“偏低”“不变”).
6.下列反应不属于取代反应的是( )
| A. | CH2=CH2+H2$\stackrel{催化剂}{→}$C2H6 | |
| B. | 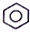 +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$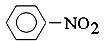 +H2O +H2O | |
| C. | CH3COOCH2CH3+H2O$→_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH | |
| D. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl |
3.下列各组物质中,属于同分异构体的是( )
| A. | O2与O3 | B. | 正戊烷与异戊烷 | C. | 甲烷与乙烷 | D. | 淀粉与纤维素 |
10.下列说法正确的是( )
| A. | 乙烯能与高锰酸钾发生取代反应而使酸性高锰酸钾溶液褪色 | |
| B. | 苯能与高锰酸钾发生取代反应而使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯能与溴单质发生加成反应而使溴水褪色 | |
| D. | 苯能与溴单质发生加成反应而使溴水褪色 |
7.油脂在NaOH稀溶液中发生皂化反应,可以判断反应基本完成的现象是( )
| A. | 反应液使酚酞试液变红色 | B. | 反应液使蓝色石蕊试纸变红色 | ||
| C. | 有大量固体析出 | D. | 反应后静置,反应液不分层 |
8.人体缺铁会引起下列哪种疾病( )
| A. | 大脖了病 | B. | 糖尿病 | C. | 痛痛病 | D. | 贫血症 |
 ⑪
⑪ ⑫
⑫