题目内容
13.下列共有十二种化学符号:①${\;}_{1}^{1}$H2 ②${\;}_{6}^{14}$C ③${\;}_{3}^{6}$Li ④${\;}_{11}^{23}$Na ⑤${\;}_{1}^{2}$H2 ⑥${\;}_{8}^{16}$O2 ⑦${\;}_{12}^{24}$Mg ⑧${\;}_{8}^{18}$O3 ⑨${\;}_{3}^{7}$Li
⑩
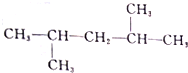 ⑪
⑪ ⑫
⑫
其中:
(1)表示核素的符号共有5种;
(2)互为同位素的是③⑨(填序号,以下相同)
(3)中子数相等,但质子数不相等的是④⑦;
(4)互为同素异形体的是⑥⑧;
(5)互为同分异构体的是⑩⑫.
分析 (1)核素是具有一定数目质子数和一定数目中子数的一类原子;
(2)质子数相同而中子数不同的同一元素的不同原子间互为同位素;
(3)中子数=质量数-质子数;
(4)同素异形体是同种元素组成的性质不同的单质之间的互称;
(5)同分异构体是分子式相同而结构不同的有机物之间的互称.
解答 解:(1)具有一定数目质子数和一定数目中子数的原子属于核素,如②③④⑦⑧⑨,故答案为:5;
(2)③⑨质子数相同,质量数不同,而中子数=质量数-质子数,所以中子数不同,③⑨互为同位素,故答案为:③⑨;
(3)中子数=质量数-质子数,④⑦的中子数均为12,但质子数不相等,故答案为:④⑦;
(4)⑥和⑧是同种氧元素组成的性质不同的单质,互称同素异形体,故答案为:⑥⑧;
(5)⑩⑫是分子式相同而结构不同的有机物,互称同分异构体,故答案为:⑩⑫.
点评 本题主要考查学生化学中的有关概念和质量数的计算,涉及同分异构体、同位素、同素异形体等,难度不大.

练习册系列答案
相关题目
3.锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源.工业上常以β锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂.其中一种工艺流程如下: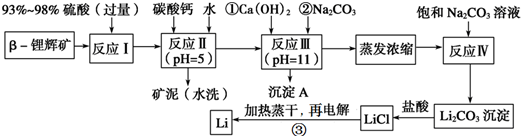
已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
请回答下列问题:
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).

已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).
4.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 18gD2O(重水)含有的质子数、电子数和中子数均为10NA | |
| B. | 2molSO2和1molO2通入密闭容器中,发生反应2SO2(g)+O2(g)$\frac{\underline{\;催化剂\;}}{△}$2SO3(g),反应完成时,生成SO3分子数小于2NA | |
| C. | 7.8gNa2O2固体含有的离子数为0.4NA | |
| D. | 2.24LH2完全燃烧时,断裂H-H键数目为0.1NA |
1.已知在25℃、1.013×105Pa条件下,1molH2在氧气中完全燃烧后放出286KJ热量,1mol水蒸气转化为液态水放出热量为44KJ.其他的相关数据如下表:
则表中a为( )
| 物质 | H2(g) | O2(g) | H2O(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/KJ | 436 | 496 | a |
| A. | 463 | B. | 260 | C. | 926 | D. | 970 |
8.下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大
②HCl溶液的酸性比H2S溶液强
③HCl的稳定性比H2S强
④还原性:Cl-<S2-
⑤HClO的酸性比H2SO4强
⑥Cl2能与H2S反应生成S
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS.
①HCl的溶解度比H2S大
②HCl溶液的酸性比H2S溶液强
③HCl的稳定性比H2S强
④还原性:Cl-<S2-
⑤HClO的酸性比H2SO4强
⑥Cl2能与H2S反应生成S
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS.
| A. | ①③④⑤ | B. | ②④⑥⑦ | C. | ③④⑥⑦ | D. | 全部 |
18.由铜片、锌片和稀硫酸组成的原电池工作时,下列叙述正确的是( )
| A. | 铜片电极反应:2H++2e-=H2↑ | B. | 锌片电极反应:Zn-e-=Zn2+ | ||
| C. | 铜为负极,发生还原反应 | D. | 锌为负极,发生还原反应 |
5.工业上用金红石(主要成分为TiO2)制金属钛,可通过以下反应进行:
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;
②TiCl4+2Mg$\frac{\underline{\;氩气\;}}{\;}$ Ti+2MgCl2;
设NA为阿伏伽德罗常数,对于上述两个反应的叙述中,正确的是( )
①TiO2+2C+2Cl2 $\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;
②TiCl4+2Mg$\frac{\underline{\;氩气\;}}{\;}$ Ti+2MgCl2;
设NA为阿伏伽德罗常数,对于上述两个反应的叙述中,正确的是( )
| A. | 两个反应都是置换反应 | |
| B. | 每生成1mol金属Ti,②中转移电子数为2NA | |
| C. | ①中TiO2作氧化剂 | |
| D. | ②中氩气作保护气,可防止金属Ti被氧化 |
2.黑火药是中国古代四大发明之一,黑火药爆炸后产物为K2S,N2,CO2,下列物质中是黑火药的主要成分且在爆炸中做还原剂的是( )
| A. | 氧气 | B. | 硫磺 | C. | 木炭 | D. | 硝酸钾 |
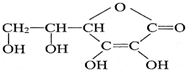 ,它的分子式是C6H8O6.在维生素C溶液中滴入少量酸性KMnO4溶液,可观察到的现象是酸性高锰酸钾颜色褪去,说明维生素C具有还原性.
,它的分子式是C6H8O6.在维生素C溶液中滴入少量酸性KMnO4溶液,可观察到的现象是酸性高锰酸钾颜色褪去,说明维生素C具有还原性.