题目内容
7.油脂在NaOH稀溶液中发生皂化反应,可以判断反应基本完成的现象是( )| A. | 反应液使酚酞试液变红色 | B. | 反应液使蓝色石蕊试纸变红色 | ||
| C. | 有大量固体析出 | D. | 反应后静置,反应液不分层 |
分析 皂化反应基本完成时生成高级脂肪酸盐和甘油均易溶于水,因此反应后静置,反应液不分层.
解答 解:皂化反应基本完成时高级脂肪酸甘油酯在碱性条件下水解生成高级脂肪酸盐和甘油均易溶于水,因此反应后静置,反应液不分层,
故选D.
点评 本题考查了油脂在碱性条件下的水解产物的性质,比较基础,掌握产物是否溶于水即可做出正确判断.

练习册系列答案
相关题目
17.在一定温度下的恒容密闭容器中,充入一定量的NO2,发生2NO2(g)?N2O4(g)反应,达到化学平衡状态的标志是( )
| A. | NO2或N2O4的浓度不再变化 | B. | c(NO2)=c(N2O4) | ||
| C. | v正(NO2)=v逆(N2O4) | D. | NO2、N2O4的总质量不再变化 |
18.由铜片、锌片和稀硫酸组成的原电池工作时,下列叙述正确的是( )
| A. | 铜片电极反应:2H++2e-=H2↑ | B. | 锌片电极反应:Zn-e-=Zn2+ | ||
| C. | 铜为负极,发生还原反应 | D. | 锌为负极,发生还原反应 |
2.黑火药是中国古代四大发明之一,黑火药爆炸后产物为K2S,N2,CO2,下列物质中是黑火药的主要成分且在爆炸中做还原剂的是( )
| A. | 氧气 | B. | 硫磺 | C. | 木炭 | D. | 硝酸钾 |
12.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1mol烃基中电子数为10NA | |
| B. | 标准状况下,11.2L乙醇中含有的分子数为0.5NA | |
| C. | 标准状况下,0.56L丙烷中含有共价键的数目为0.2NA | |
| D. | 0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6NA |
17.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
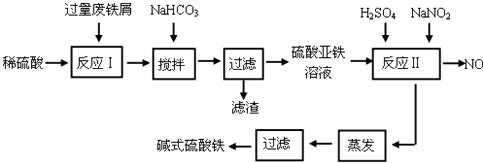
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在4.4~7.5范围内,使溶液中的Al3+沉淀(写离子符号).
(2)反应Ⅱ中加入NaNO2的目的是氧化Fe2+,发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O=Fe2(OH)42++2H+.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH在4.4~7.5范围内,使溶液中的Al3+沉淀(写离子符号).
(2)反应Ⅱ中加入NaNO2的目的是氧化Fe2+,发生反应的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.
(3)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为2Fe(OH)2++2H2O=Fe2(OH)42++2H+.


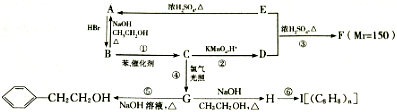
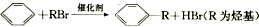 ;
; 可以在铁、稀盐酸作用下生成
可以在铁、稀盐酸作用下生成 ;
; .
.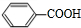 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$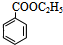 +H2O;
+H2O; ;
;
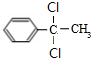 .
.