题目内容
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤I:称取样品1.500g.
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数______(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积______(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察______.
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______色变成______色.
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010mol?L-1,则该样品中氮的质量分数为______.
步骤I:称取样品1.500g.
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数______(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积______(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察______.
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______色变成______色.
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
(1)①碱式滴定管用蒸馏水洗涤后需要再用NaOH溶液润洗,否则相当于NaOH溶液被稀释,滴定消耗的体积会偏高,测得样品中氮的质量分数也将偏高,
故答案为:偏高;
②锥形瓶用蒸馏水洗涤后,虽然水未倒尽,但待测液中的H+的物质的量不变,则滴定时所需NaOH标准溶液中的氢氧化钠的物质的量就不变,也就是无影响,
故答案为:无影响;
③定时边滴边摇动锥形瓶,眼睛应注意观察颜色变化,确定滴定终点,故答案为:B;
④待测液为酸性,酚酞应为无色,当溶液转为碱性时,溶液颜色变为粉红(或浅红),故答案为:浅红;
(2)标准溶液的体积应取三次实验的平均值,
首先确定滴定时所用的NaOH标准溶液为
mL=20.00mL,
根据题意中性甲醛溶液一定是过量的,而且1.500g 铵盐 经溶解后,取了其中
进行滴定,即0.15g,
滴定结果,溶液中含有H+(含(CH2)6N4H+)共0.02L××0.1010mol/L=0.00202mol,
根据4NH4++6HCHO═3H++6H2O+(CH2)6N4H+,每生成4molH+(含(CH2)6N4H+),会消耗NH4+4mol,
所以共消耗NH4+0.00202mol,
其中含氮元素0.00202mol×14g/mol=0.02828g
所以氮的质量分数为
×100%=18.85%,
故答案为:18.85%.
故答案为:偏高;
②锥形瓶用蒸馏水洗涤后,虽然水未倒尽,但待测液中的H+的物质的量不变,则滴定时所需NaOH标准溶液中的氢氧化钠的物质的量就不变,也就是无影响,
故答案为:无影响;
③定时边滴边摇动锥形瓶,眼睛应注意观察颜色变化,确定滴定终点,故答案为:B;
④待测液为酸性,酚酞应为无色,当溶液转为碱性时,溶液颜色变为粉红(或浅红),故答案为:浅红;
(2)标准溶液的体积应取三次实验的平均值,
首先确定滴定时所用的NaOH标准溶液为
| 20.01+19.99+20.00 |
| 3 |
根据题意中性甲醛溶液一定是过量的,而且1.500g 铵盐 经溶解后,取了其中
| 1 |
| 10 |
滴定结果,溶液中含有H+(含(CH2)6N4H+)共0.02L××0.1010mol/L=0.00202mol,
根据4NH4++6HCHO═3H++6H2O+(CH2)6N4H+,每生成4molH+(含(CH2)6N4H+),会消耗NH4+4mol,
所以共消耗NH4+0.00202mol,
其中含氮元素0.00202mol×14g/mol=0.02828g
所以氮的质量分数为
| 0.02828 |
| 0.15 |
故答案为:18.85%.

练习册系列答案
相关题目
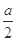 g
g 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+