题目内容
【题目】以下是某药物中间体D的合成过程:
A(C6H6O)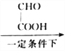 B
B![]()

![]()

(1)A的结构简式为_________________,A转化为B的反应类型是____________。
(2)D中含氧官能团的名称是__________。
(3)鉴别B、C可以用的试剂名称是______________。
(4)D在一定条件下与足量NaOH溶液反应的化学方程式是_________________。
(5)同时符合下到条件的D的所有同分异构体(不考虑立体异构)有________种。
①能与NaHCO3溶液反应产生气体;②苯环上只有2个取代基;③遇氯化铁溶液发生显色反应。其中核磁共振氢谱显示为5组峰,且峰面积比为3∶1∶2∶2∶1的同分异构体的结构简式是________________________________(写结构简式)。
(6)已知:
 +CH≡CH
+CH≡CH 
请设计合成路线以A和C2H2为原料合成![]() (无机试剂任选):____________。
(无机试剂任选):____________。
【答案】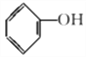 加成反应 (酚)羟基、酯基 碳酸氢钠
加成反应 (酚)羟基、酯基 碳酸氢钠 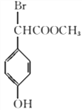 +3NaOH
+3NaOH![]()
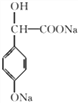 +CH3OH+NaBr+H2O 12
+CH3OH+NaBr+H2O 12 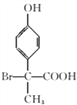
【解析】
本题考查有机物的推断和合成,(1)根据C的结构简式,判断出B生成C反应类型为酯化反应,即B的结构简式为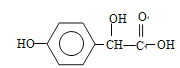 ,根据A的分子式,以及B的结构简式,推出A为苯酚,结构简式为
,根据A的分子式,以及B的结构简式,推出A为苯酚,结构简式为 ,结合A和B的结构简式,A生成B的反应类型为加成反应;(2)根据D的结构简式,含有含氧官能团是酯基和(酚)羟基;(3)B含有羧基,C不含有羧基,且酚羟基电离出H+能力小于碳酸,羧酸的酸性强于碳酸,因此检验两种物质,可以滴加NaHCO3溶液,B溶液中出现气泡,C中不出现气泡;(4)根据氢氧化钠发生反应的是酚羟基、酯基、溴原子,因此发生的反应方程式为
,结合A和B的结构简式,A生成B的反应类型为加成反应;(2)根据D的结构简式,含有含氧官能团是酯基和(酚)羟基;(3)B含有羧基,C不含有羧基,且酚羟基电离出H+能力小于碳酸,羧酸的酸性强于碳酸,因此检验两种物质,可以滴加NaHCO3溶液,B溶液中出现气泡,C中不出现气泡;(4)根据氢氧化钠发生反应的是酚羟基、酯基、溴原子,因此发生的反应方程式为 +3NaOH
+3NaOH![]()
 +CH3OH+NaBr+H2O;(5)能与NaHCO3溶液产生气体,则结构中含有羧基,遇FeCl3溶液发生显色反应,说明含有酚羟基,符合条件的同分异构体为
+CH3OH+NaBr+H2O;(5)能与NaHCO3溶液产生气体,则结构中含有羧基,遇FeCl3溶液发生显色反应,说明含有酚羟基,符合条件的同分异构体为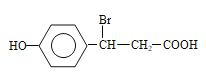 (邻间对三种)、
(邻间对三种)、 (邻间对三种)、
(邻间对三种)、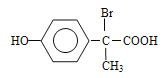 (邻间对三种)、
(邻间对三种)、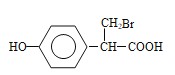 (邻间对三种),共有12种;核磁共振氢谱有5种峰,说明有5种不同的氢原子,即结构简式为
(邻间对三种),共有12种;核磁共振氢谱有5种峰,说明有5种不同的氢原子,即结构简式为 ;(6)根据信息,生成
;(6)根据信息,生成![]() 的反应物应是乙炔和
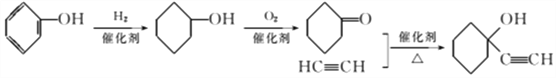
的反应物应是乙炔和![]() ,因此先让A与氢气发生加成反应,然后再被氧化,合成路线为
,因此先让A与氢气发生加成反应,然后再被氧化,合成路线为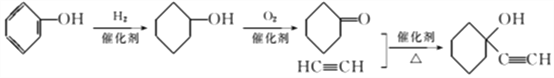 。
。

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】亚硝酰氯是工业上重要的原料,是合成有机物的中间体。
2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0
2ClNO(g) △H<0
(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1 ,则平衡后NO的转化率α1=_____________。其它条件保持不变,反应在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”)。
(2)若使反应2NO(g)+Cl2(g)![]() 2ClNO(g) 的平衡常数增大,可采用的措施是___________。
2ClNO(g) 的平衡常数增大,可采用的措施是___________。
(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g)![]() 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。

(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
容器编号 | 温度/℃ | 容器体积/L | 平衡时ClNO含量(占比) |
Ⅰ | T1 | 2 | 2/3 |
Ⅱ | T2=T1 | 3 | W2 |
Ⅲ | T3>T1 | V3 | 2/3 |
Ⅳ | T4 | V4 | W4 |
Ⅴ | T5 | V5 | W5 |
①V3________2 (填写“大于”、“小于”或“等于”);
②容器Ⅱ中化学平衡常数K=_________;
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是_____________________;容器Ⅴ与容器Ⅰ的体积不同,则容器Ⅴ中反应达到平衡时气体总压强(P )的范围是________。

【题目】NO2是大气污染物,但只要合理利用也是重要的资源。回答下列问题:
(1)NO2可以被NaOH溶液捕获生成两种钠盐,溶液呈碱性,写出反应的化学方程式______________,已知常温下,HNO2的电离平衡常数为Ka=5.0×10-4,则0.1mo/L NaNO2中c(OH-)=_____________(已知![]() )
)
(2)2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步,反应情况如下表:
2NO2(g)的反应历程分两步,反应情况如下表:
反应 | 速率表达式 | 反应热 |
反应I:2NO(g) |
| △H1<0 |
反应II:N2O2(g)+O2(g) |
| △H2<0 |
反应2NO(g)+O2(g) ![]() 2NO2(g)的△H______(用△H1、△H2表示)。一定温度下,反应2NO(g)+O2(g)
2NO2(g)的△H______(用△H1、△H2表示)。一定温度下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,若升高温度,K将____(填“增大”、“减小”或“不变”),平衡常数的表达式K=____(用
2NO2(g)达到平衡状态,若升高温度,K将____(填“增大”、“减小”或“不变”),平衡常数的表达式K=____(用![]() 、
、![]() 、
、![]() 、
、![]() 表示)
表示)
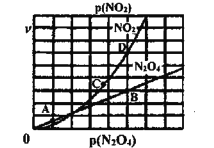
(3)反应N2O4(g) ![]() 2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强关系为:υ(N2O4)=k1· p(N2O4),υ(NO2)=k2· p(NO2),其中
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强关系为:υ(N2O4)=k1· p(N2O4),υ(NO2)=k2· p(NO2),其中![]() 、
、![]() 是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态对应的两个点是___________
是与温度有关的常数。一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态对应的两个点是___________
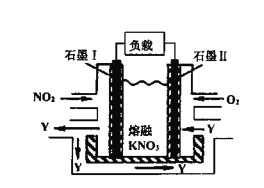
(4)NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。Y的化学式为____________