题目内容
【题目】亚硝酰氯是工业上重要的原料,是合成有机物的中间体。
2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0
2ClNO(g) △H<0
(1)在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1 ,则平衡后NO的转化率α1=_____________。其它条件保持不变,反应在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”)。
(2)若使反应2NO(g)+Cl2(g)![]() 2ClNO(g) 的平衡常数增大,可采用的措施是___________。
2ClNO(g) 的平衡常数增大,可采用的措施是___________。
(3)将NO与Cl2按物质的量之比2∶1充入一绝热密闭容器中,发生反应:2NO(g)+Cl2(g)![]() 2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。
2ClNO △H<0,实验测得NO的转化率α(NO)随时间的变化经如图所示。NO(g)的转化率α(NO)在t2~t3时间段内降低的原因是______________________________。

(4)在其他条件相同时,向五个恒温的密闭容器中分别充入1molCl2与2molNO,发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
2ClNO(g) △H< 0,部分反应条件及平衡时ClNO的含量如下表所示:
容器编号 | 温度/℃ | 容器体积/L | 平衡时ClNO含量(占比) |
Ⅰ | T1 | 2 | 2/3 |
Ⅱ | T2=T1 | 3 | W2 |
Ⅲ | T3>T1 | V3 | 2/3 |
Ⅳ | T4 | V4 | W4 |
Ⅴ | T5 | V5 | W5 |
①V3________2 (填写“大于”、“小于”或“等于”);
②容器Ⅱ中化学平衡常数K=_________;
③容器Ⅳ、容器Ⅴ分别与容器Ⅰ相比实验条件不同,反应体系总压强随时间的变化如图所示。与容器Ⅰ相比,容器Ⅳ改变的实验条件是_____________________;容器Ⅴ与容器Ⅰ的体积不同,则容器Ⅴ中反应达到平衡时气体总压强(P )的范围是________。

【答案】75% > 降低温度 t2达到平衡,t2~t3段温度升高,平衡逆向移动,NO转化率减小 小于 72 使用催化剂 6Mpa<P<6.75Mpa
【解析】
(1)考查化学平衡的计算,根据化学反应速率的数学表达式,生成ClNO的物质的量为7.5×10-3×10×2mol=0.15mol,消耗的NO的物质的量为0.15mol,NO的转化率为0.15/0.2×100%=75%,恒容状态,反应向正反应方向进行,气体物质的量减少,压强减小,向正反应趋向减小,恒压状态下,压强不变,向正反应方向趋向比恒容大,即α2>α1;(2)考查影响化学平衡常数的因素,正反应是放热反应,降低温度平衡向正反应方向移动,化学平衡常数增大,因此采用措施为降低温度;(3)考查勒夏特列原理,t2时刻NO的转化率最大,说明反应达到平衡,即0~t2时刻反应向正反应方向进行,正反应方向是放热反应,t2时刻后,温度升高,平衡向逆反应方向移动,NO的转化率降低;(4)考查化学平衡常数的计算、勒夏特列原理,①T3>T1,在T1的基础上升高温度到T3,正反应方向是放热反应,平衡向逆反应方向进行,ClNO的量降低,但III和I容器中ClNO的含量相等,III中容器的体积小于I容器,因此V3<2L;②2NO(g)+Cl2(g)![]() 2ClNO(g)
2ClNO(g)
起始: 2 1 0
变化: 2x x 2x
平衡:2-2x 1-x 2x I容器达到平衡时,ClNO的含量为2/3,因此有![]() ,解得x=0.75,根据化学平衡常数的定义,K=
,解得x=0.75,根据化学平衡常数的定义,K=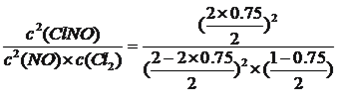 =72,化学平衡常数只受温度的影响,容器II中温度与容器I的温度相等,因此容器II中化学平衡常数为72;③根据图像,IV比I先达到化学平衡,说明IV的化学反应速率比I快,达到平衡是IV和I压强相同,说明该因素只影响化学反应速率,不影响化学平衡的移动,因此改变的实验条件是使用催化剂;令V容器中消耗Cl2的物质的量为ymol,利用PV=nRT,起始时
=72,化学平衡常数只受温度的影响,容器II中温度与容器I的温度相等,因此容器II中化学平衡常数为72;③根据图像,IV比I先达到化学平衡,说明IV的化学反应速率比I快,达到平衡是IV和I压强相同,说明该因素只影响化学反应速率,不影响化学平衡的移动,因此改变的实验条件是使用催化剂;令V容器中消耗Cl2的物质的量为ymol,利用PV=nRT,起始时 ,达到平衡后,
,达到平衡后, ,得出y=3-P/3,V容器压强大于I,平衡向正反应方向进行,y>0.75,即3-P/3>0.75,解得P<6.75,根据压强与时间的关系,推出P的范围是6Mpa<P<6.75Mpa。
,得出y=3-P/3,V容器压强大于I,平衡向正反应方向进行,y>0.75,即3-P/3>0.75,解得P<6.75,根据压强与时间的关系,推出P的范围是6Mpa<P<6.75Mpa。